
 2C(g),该反应达到平衡时,平衡混和气中A的体积分数为( )
2C(g),该反应达到平衡时,平衡混和气中A的体积分数为( )| A.50% | B.60% | C.70% | D.无法计算 |
 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案科目:高中化学 来源:不详 题型:单选题
 (CH3COOH)2(气)+热。现欲测定乙酸的分子量,应采用的反应条件是( )
(CH3COOH)2(气)+热。现欲测定乙酸的分子量,应采用的反应条件是( )| A.低温高压 | B.高温低压 | C.低温低压 | D.高温高压 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2Z(g);
2Z(g); H<0,达到平衡时,下列说法正确的是
H<0,达到平衡时,下列说法正确的是| A.减小容器体积,平衡向右移动 | B.加入催化剂,Z的产率增大 |
| C.增大c(X),X的转化率增大 | D.降低温度,Y的转化率增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2SO3(g) △H<0达平衡后,采用下列措施一段时间后,既能增大逆反应速率又能使平衡向正方向移动的是
2SO3(g) △H<0达平衡后,采用下列措施一段时间后,既能增大逆反应速率又能使平衡向正方向移动的是| A.通入大量O2 | B.增大容器容积 | C.移去部分SO3 | D.降低体系温度 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
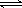 H2(g)+I2(g)已达平衡状态的是
H2(g)+I2(g)已达平衡状态的是 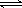 2SO3(g)。研究发现,
2SO3(g)。研究发现,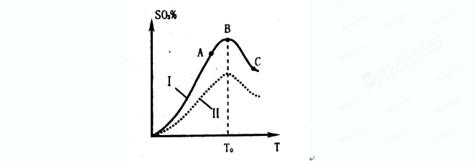
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.升高温度,水的电离平衡向正方向移动 |
| B.合成氨工业选择高温 |
| C.增大压强,有利于SO2和O2反应生成SO3 |
D.在Fe3++3KSCN Fe(SCN)3反应达平衡时,增加KSCN的浓度,体系颜色变深 Fe(SCN)3反应达平衡时,增加KSCN的浓度,体系颜色变深 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
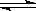 2SO3(g) 是可逆反应的事实是
2SO3(g) 是可逆反应的事实是| A.O2仍为1mol | B.SO2仍为2mol |
| C.SO2完全转化为 SO3 | D.SO2、O2、 SO3同时存在 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2Q (g) + nR (g),达到平衡后,容器内温度不变,混合气体的压强比原来增加5%,X的浓度减小1/3,则该反应方程式中的n值( )
2Q (g) + nR (g),达到平衡后,容器内温度不变,混合气体的压强比原来增加5%,X的浓度减小1/3,则该反应方程式中的n值( )| A.4 | B.5 | C.6 | D.7 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

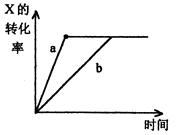
| A.减小Y的浓度 |
| B.增大Y的浓度 |
| C.降低温度 |
| D.减小反应体系的压强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com