
下列叙述或表示正确的是( )
| A.常温下pH均为3的醋酸和硫酸的水溶液,分别加水稀释100倍后,两种溶液的pH仍相同 |
| B.氢氧化钙溶液中加入过量的碳酸氢钙溶液的离子方程式:Ca2+ + HCO3—+OH— = CaCO3 ↓+ H2O |
| C.Ksp反映了难熔电解质在水中的溶解能力,它的大小与浓度无关,与温度无关。 |
| D.c(H+)=1×10-2 mol·L的溶液:Fe2+、Ba2+、N03-、Cl-不能大量共存。 |
D
解析试题分析:A. 醋酸是弱酸,部分电离,C(CH3COOH)>C(H+)。当加谁呢稀释时,会使电离平衡向电离的方向移动,导致C(H+)又有所增加;硫酸是强酸,完全电离。加水稀释,C(H+)只是减小,所以常温下将pH均为3的醋酸和硫酸的水溶液,分别加水稀释100倍后,两种溶液的pH硫酸的大于醋酸的。错误。B.酸式盐与碱发生反应时要以不足量的物质为标准。氢氧化钙溶液中加入过量的碳酸氢钙溶液的离子方程式:Ca2+ +2OH—+2 HCO3—= CaCO3 ↓+ 2H2O+ CO32-。错误。C. Ksp反映了难熔电解质在水中的溶解能力,它的大小与浓度无关,与温度有关。错误。D.c(H+)=1×10-2 mol·L的溶液是酸性溶液这时:H+、Fe2+、N03-会发生离子反应而不能大量共存。正确。
考点:考查离子方程式的书写、离子共存、电解质溶液的稀释及影响Ksp的因素的知识。


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:单选题
下列各溶液中,物质的量浓度关系正确的是
| A.0.1 mol?L—1的KAl(SO4)2溶液中:c(SO42—)>c(K+)>c(A13+)>c(H+)>c(OH—) |
| B.10mL0.01mo1?L—1HCl溶液与10mL0.01mo1?L—1Ba(OH)2溶液充分混合,若混合后溶液的体积为20mL,则溶液的pH=12 |
| C.在01mo1?L—1CH3COONa溶液中,c(OH—)=c(CH3COOH)+c(H+) |
| D.等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液,若溶液呈酸性,则有c(Na+)>c(HX)>c(X—)>c(H+)>c(OH—) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期元素W、X、Y、Z的原子序数依次增大,它们的简单离子中都能破坏水的电离的组合是
| A.Y3+、W- | B.Z2-、X+ | C.X+、Y3+ | D.X+、Z2- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
25℃时,弱酸的电离平衡常数如下表,下列表述错误的是
| 弱酸 | CH3COOH | HCN | H2CO3 |
| K | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法不正确的是
| A.将pH=4的某酸稀释10倍,测得其pH<5,则该酸为弱酸 |
B.0.1mol 的NaHCO3溶液中 的NaHCO3溶液中 |
C.0.1mol 的NaHA溶液Ph=5,则溶液: 的NaHA溶液Ph=5,则溶液: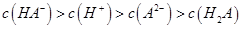 |
D.pH=4的醋酸与pH=10的氢氧化钠溶液等体积混合,所得溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知:25℃时,Ksp[Mg(OH)2]=5.61×10-12,Ksp[MgF2]=7.42×10-11。下列说法正确的是
| A.25℃时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的c(Mg2+)小 |
| B.25℃时,向Mg(OH)2的澄清饱和溶液中加入少量的NH4Cl固体,c(Mg2+)降低 |
| C.25℃时,Mg(OH)2固体在20 mL 0.01 mol/L氨水中的Ksp比在20 mL 0.01 mol/LNH4Cl溶液中的Ksp小 |
| D.25℃时,在Mg(OH)2悬浊液中加入NaF溶液后,Mg(OH)2不可能转化为MgF2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在一定条件下发生下列反应,其中属于盐类水解反应的是
A.NH4++2H2O NH3·H2O+H3O+ NH3·H2O+H3O+ |
B.HCO3-+ H2O H3O+ + CO32- H3O+ + CO32- |
| C.HS-+H+= H2S |
D.Cl2+H2O  H++Cl-+HclO H++Cl-+HclO |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列溶液中有关物质的浓度关系正确的是 ( )
| A.c(NH4+)相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液中:c(NH4HSO4) >c[(NH4)2SO4]>c(NH4Cl) |
| B.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| C.1.0 mol/L Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) |
| D.某二元弱酸酸式盐NaHA溶液中:c(H+)+c(Na+)=c(OH-)+c(HA-)+c(A2-) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某酸性溶液中只有Na+、CH3COO-、H+、OH-四种离子。则下列描述正确的是
| A.该溶液由pH=3的CH3COOH与pH=11的NaOH溶液等体积混合而成 |
| B.该溶液由等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合而成 |
| C.加入适量NaOH,溶液中离子浓度为c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
| D.加入适量氨水,c(CH3COO-)一定大于c(Na+)、c(NH4+)之和 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com