
【题目】(1)支链有一个乙基且相对分子质量最小的烷烃的分子式为________
(2)分子中含有25个共价键且一氯代物只有一种的烷烃结构简式是________
(3)某饱和链状有机物分子中含有n个﹣CH3,b个﹣CH2﹣,m个![]() ,a个
,a个 ![]() ,其余为﹣Cl,则﹣Cl的数目是________
,其余为﹣Cl,则﹣Cl的数目是________
(4)某烃A 0.2 mol在氧气中充分燃烧后,生成化合物CO2、H2O各1.2 mol,试回答:
①烃A的分子式是________。
②若烃A能使溴水褪色,在催化剂作用下与H2发生加成反应后生成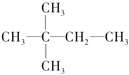 ,对A进行命名,其名称为________。
,对A进行命名,其名称为________。
③若烃A能使溴水褪色,且分子中所有碳原子共平面,则A的结构简式为________。
【答案】 C7H16 (CH3)3CC(CH3)3 m+2a+2﹣n C6H12 3,3-二甲基-1-丁烯 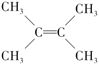
【解析】(1)支链只有一个乙基,主链至少含有5个C;式量最小的烷烃含有7个C,该有机物的结构简式为:CH(C2H5)3,分子式为: C7H16。答案:C7H16。
(2) 设烷烃分子式为CnH2n+2,分子中含有25个共价键,所以2n+2+n-1=25,n=8,一氯代物只有一种的是完全对称式,所以它的结构简式是C(CH3)3C(CH3)3。答案:(CH3)3CC(CH3)3。
(3)若只连接甲基,﹣CH2﹣不管多少个只能连接两个﹣CH3,m个![]() ,能连接m个﹣CH3; a个
,能连接m个﹣CH3; a个 ![]() 能连接2a个﹣CH3;根据b个﹣CH2﹣,m个-CH-, a个
能连接2a个﹣CH3;根据b个﹣CH2﹣,m个-CH-, a个 ![]() ;连接n个﹣CH3, 因为是饱和链状有机物,所以连接的Cl数为2+m+2a-n个;答案: 2+m+2a=n。
;连接n个﹣CH3, 因为是饱和链状有机物,所以连接的Cl数为2+m+2a-n个;答案: 2+m+2a=n。
(4)①因为烃只含有C、H两种元素,某烃A 0.2 mol在氧气的充分燃烧后生成化合物CO2、H2O各1.2 mol,则1mol烃中含有6mol,12mol原子,分子式为C6H12;本题正确答案是: C6H12。
②若烃A能使溴水褪色,在催化剂作用下与H2加成生成![]() ,说明分子中含有1个C=C键,相邻两个碳原子都含有H原子为C=C,双键位置,故A的结构简式为: (CH3)3CCH=CH2, 其名称为:3,3-二甲基-1-丁烯,本题答案: 3,3-二甲基-1-丁烯。
,说明分子中含有1个C=C键,相邻两个碳原子都含有H原子为C=C,双键位置,故A的结构简式为: (CH3)3CCH=CH2, 其名称为:3,3-二甲基-1-丁烯,本题答案: 3,3-二甲基-1-丁烯。
③若烃A能使溴水褪色,含有不饱和双键,且分子中所有碳原子共平面,说明A中含有C=C,根据A的分子式为C6H12,则A的结构简式为![]() 。答案:
。答案:![]() 。
。


 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案科目:高中化学 来源: 题型:
【题目】我国知名企业比亚迪公司开发了具有多项专利的锂钒氧化物二次电池,其成本较低,对环境无污染,能量密度远远高于其它材料电池,电池总反应为:V2O5+xLi![]() LixV2O5。下列说法中正确的是
LixV2O5。下列说法中正确的是
A.锂在放电时做正极材料,充电时为阳极材料
B.电池在放电时,Li+向负极移动
C.该电池充电时阳极的反应为:LixV2O5 -xe-=V2O5 + xLi+
D.V2O5只是锂发生反应的载体,不参与电池反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是实验室进行氨气快速制备与性质实验的组合装置,部分固定装置未画出. 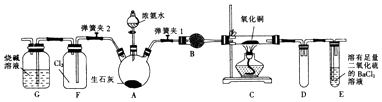
(1)在组装好装置之后,应进行的操作名称是 .
(2)装置B中盛放的试剂是 .
(3)当C中固体全部变为红色后,关闭弹簧夹1,慢慢移开酒精灯,待冷却后,称量C中固体质量,若反应前固体质量为16g,反应后固体质量减少2.4g,则该固体产物的成分是(用化学式表示).从E中逸出液面的气体可以直接排入空气中,请写出在C中发生反应的化学方程式: .
(4)关闭弹簧夹1,打开弹簧夹2,气体进入F中立即产生白烟,同时发现G中溶液迅速倒吸流入F中.请写出产生白烟的化学方程式: , 迅速发生倒吸的原因是 .
(5)为了证明一水合氨是弱碱,甲、乙两同学分别设计如下实验进行探究. ①甲同学用pH试纸测得室温下0.01molL﹣1氨水的pH为10,则认定一水合氨是弱电解质,理由是 .
②乙同学取出10mL 0.1molL﹣1氨水,滴入2滴酚酞试液,溶液显粉红色,再加入少量NH4Cl晶体,观察到 , 证明一水合氨是弱电解质.
③请设计一个与甲、乙同学不同的简单实验方案,证明一水合氨是弱电解质: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某稀溶液中含有4 mol KNO3和2.5 mol H2SO4,向其中加入1.5 mol Fe,充分反应(已知NO![]() 被还原为NO),最终溶液体积为1L。下列说法正确的是( )
被还原为NO),最终溶液体积为1L。下列说法正确的是( )
A. 反应后生成NO的体积为33.6 L (标况)
B. 所得溶液中c(Fe2+)∶c(Fe3+)=1∶2
C. 所得溶液中c(NO![]() )=2.75 mol·L-1
)=2.75 mol·L-1
D. 所得溶液中的溶质只有FeSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高炉煤气是炼铁厂排放的尾气,含有H2、N2、CO、CO2及O2,其中N2约为55%、CO约为25%、CO2约为15%、O2约为1.64% (均为体积分数)。某科研小组对尾气的应用展开研究:
I.直接作燃料
己知:C(s)+O2(g)=CO2 (g) △H=-393.5kJ/mol
2C(s)+O2(g)=2CO (g) △H=-221kJ/mol
(1)CO燃烧热的热化学方程式为____________________________________________________________________________ 。
II.生产合成氨的原料
高炉煤气经过下列步骤可转化为合成氨的原料气:
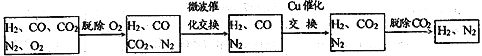
在脱氧过程中仅吸收了O2;交换过程中发生的反应如下,这两个反应均为吸热反应:CO2+CH4![]() CO+H2 CO+H2O
CO+H2 CO+H2O![]() CO2+ H2
CO2+ H2
(2)气体通过微波催化交换炉需要较高温度,试根据该反应特征,解释采用较高温度的原因:____________________________________________________________________________ 。
(3)通过铜催化交换炉后,所得气体中V(H2):V(N2)= ______________。
III.合成氨后的气体应用研究
(4)氨气可用于生产硝酸,该过程中会产生大气污染物NOx。为了研究对NOx的治理,该科研小组在恒温条件下,向2L恒容密闭容器中加入0.2molNO 和0.1molCl2,发生如下反应:2NO(g)+Cl2(g)![]() 2ClNO(g) △H<0。10min时反应达平衡,测得10min 内v (ClNO)=7.5
2ClNO(g) △H<0。10min时反应达平衡,测得10min 内v (ClNO)=7.5![]() 10-3mol/(L·min),则平衡后n(Cl2)=_________mol。
10-3mol/(L·min),则平衡后n(Cl2)=_________mol。
设此时NO的转化率为α1,若其它条件不变,上述反应在恒压条件下进行,平衡时NO 的转化率为α2,则α1 ____α2 (填“>”、“<”或“=”);平衡常数K____ (填增大”“减小 ”或“不变”)
(5)氨气还可用于制备NCl3,NCl3发生水解产物之一具有强氧化性,该水解产物能将稀盐酸中的NaClO2氧化成ClO2,该反应的离子方程式为_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1981年,Thoms Cech在研究四膜虫时,发现其rRNA前体加工除去某些片段的过程中发生“剪接反应”,该反应是在仅有RNA没有任何蛋白质参与的情况下完成的。下列推论最合理的是( )
A.该反应不需要酶的催化 B.四膜虫体内的这种RNA具有酶的特性
C.所有蛋白质和RNA都是酶 D.有的DNA也可能是酶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知: 2H2 (g)+O2 (g)=2H2O(l) △H= a kJ/mol,2H2 (g)+O2 (g)=2H2O(g) △H= b kJ/mol,则a、b的大小关系是
A.a=bB.a>bC.a<bD.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列提供的一组物质回答问题:
①NH4Cl ②MgCl2 ③H2S ④Na2O2 ⑤MgO ⑥Cl2 ⑦NaOH ⑧CH4 ⑨NH3 ⑩CO2
(1)仅含有共价键的是_____;既有离子键又有共价键的是_____(用序号表示)
(2)离子化合物有_____;共价化合物有______(用序号表示)
(3)MgCl2 的电子式______;NH3 的电子式_____;Na2O2 的电子式_____
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com