
下列说法不正确的是
A.氯化钠晶体中,每个Cl-周围最近且距离相等的Cl-共有12个
B.分子晶体中有范德华力,也有共价键
C.干冰晶体中,每个CO2分子周围最近且距离相等的CO2分子共有12个
D.晶体熔点:晶体硅<SiC
B
【解析】
试题分析:A.氯化钠晶体中,每个Cl-周围最近且距离相等的Cl-的个数是:(3×8)÷2=12个。正确。B.在分子晶体中有范德华力,若分子为单原子分子,则分子内无共价键,若为双原子分子或多原子分子,则也有共价键。错误。C.干冰晶体中,每个CO2分子周围最近且距离相等的CO2分子个数为:(3×8)÷2=12个。正确。D.晶体Si、SiC但是原子晶体。对于原子晶体来说,共价键的键长越短,则共价键结合的就越牢固,断裂消耗的能量就越高,熔沸点就越高。而键长取决于形成共价键的原子半径,由于原子半径Si>C,晶体熔点:晶体硅<SiC。正确。
考点:考查晶体中含有的作用力、微粒的配位数、熔沸点的比较的知识。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2013-2014福建省高二下学期期末考试化学试卷(解析版) 题型:填空题
铁及其化合物与生产、生活关系密切。
(1)下图是实验室研究海水对铁闸不同部位腐蚀情况的剖面示意图。
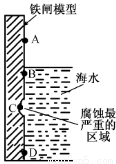
①该电化腐蚀称为 。
②图中A和B区域相比较,腐蚀较慢的是 (填字母)。
(2)实验室经常用到FeCl3溶液,在配制FeCl3溶液时常需加入少量 的 ;将FeCl3溶液和碳酸氢钠溶液混合,将产生红褐色沉淀和无色气体,该反应的离子方程式为 。
(3)已知t℃时,反应FeO(s)+CO(g) Fe( s) +CO2(g)的平衡常数K= 0.25。
Fe( s) +CO2(g)的平衡常数K= 0.25。
①t℃时,反应达到平衡时n(CO2):n(CO)=
②若在1L密闭容器中加人0.02 mol FeO(s),并通入x mol CO,t℃时反应达到平衡。此时
FeO(s)转化率为50%,则x= 。
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省高一下学期期末考试化学试卷(解析版) 题型:选择题
下列各组物质中,每种物质都是既有离子键又有共价键的一组是( )
A.NaOH H2SO4 (NH4)2SO4 B.MgO Na2SO4 HNO3
C.Na2O2 KOH Na3PO4 D.HCl Na2O MgCl2
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省三明市三校高三下学期联考理综化学试卷(解析版) 题型:选择题
下列离子方程式中正确的是
A.向NaAlO2 溶液中通入过量CO2:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
B.硫化钠的水解反应:S2-+H3O+ HS-+H2O
HS-+H2O
C.1 mol/L的KAl(SO4) 2溶液与2 mol/L的Ba(OH) 2溶液等体积混合:Al3++4OH—= AlO2—+2H2O
D.用食醋溶解水垢:2H++CaCO3=Ca2++H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省“四地六校”下学期第三次联考高二化学试卷(解析版) 题型:填空题
(13分)C和Si分别是构成生命体和岩石的重要元素。
(1)CH4和SiH4沸点较高的是 。原因是 。稳定性较高的是 。
(2)SiC的晶体结构与晶体硅相似,其中C原子的杂化方式为 。微粒间存在的作用力是 。
(3)CO2形成的干冰晶体与SiO2晶体相比,下列说法不正确的有 。
A中心原子的杂化方式不同 B构成晶体的微粒种类不同 C晶体内微粒间作用力不同
D晶体导电性不同 E.常温时,晶体挥发性不同
(4)已知键能数据如下,化学反应的ΔH等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。写出Si(s)在O2中燃烧生成SiO2(s)的热化学方程式 。
化学键 | Si—O | O=O | Si—Si |
键能(kJ·mol-1) | 460 | 498 | 226 |
(5)氨基酸是构成蛋白质的物质基础,甘氨酸H2N-CH2-COOH中,各元素的电负性从大到小为 。
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省“四地六校”下学期第三次联考高二化学试卷(解析版) 题型:选择题
现代无机化学对硫-氮化合物的研究是最为活跃的领域之一。其中下图是已经合成的最著名的硫-氮化合物的分子结构。下列说法正确的是
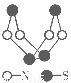
A.该物质的分子式为SN B.该物质的晶体中微粒间作用力有2种
C.该物质具有很高的熔、沸点 D.该物质与化合物S2N2互为同素异形体
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省“四地六校”下学期第三次联考高二化学试卷(解析版) 题型:选择题
下列现象不能用氢键解释的是
A.冰的密度比水小,浮于水面 B.氨气易液化
C.乙醇极易溶于水 D.碘易溶于苯(C6H6)
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省“四地六校”下学期第三次联考高一化学试卷(解析版) 题型:选择题
下列化合物中,阴离子和阳离子的半径之比最大的是 ( )
A.CsI B. NaF C. LiI D. KCl
查看答案和解析>>
科目:高中化学 来源:2013-2014甘肃省高二下学期期末考试化学试卷(解析版) 题型:选择题
某有机物的结构简式如图所示,下列说法不正确的是( )
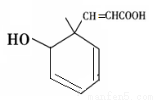
A.分子式为C10H12O3
B.含有3种官能团
C.1 mol该分子中含有3 mol双键
D.既可以发生取代反应又可以发生加成反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com