
现有以下5种说法:①胶体是纯净物;②盐酸和食醋既是化合物又是酸;③次氯酸、烧碱、纯碱依次分别为酸、碱、盐;④青铜器、钱币等均是合金;⑤CO为酸性氧化物。其中错误的是
A.①②⑤ B.①②③④⑤
C.③④ D.②⑤
科目:高中化学 来源: 题型:
某化学学习小组为了解硫酸及其盐的某些性质和用途,进行了如下实验探究。
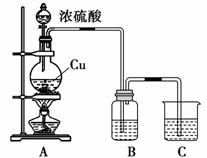
[实验一] 探究浓硫酸的氧化性:
(1)写出烧瓶中反应的化学方程式:____________________________________。
(2)B装置可用于探究SO2的还原性,则B中所用的试剂为:________________(任写一种即可);若B装置是品红溶液,则B中的现象是_______________________________。
[实验二] 检验(NH4)2Fe(SO4)2·6H2O中的金属离子:
(3)请结合化学用语和必要的文字说明如何检验出其中的金属离子(试剂、原理、现象等):______________________________________________________________________。
[实验三] 用KHSO4制取H2O2并测其质量分数:
查阅资料得知:工业上用如下原理制取H2O2:
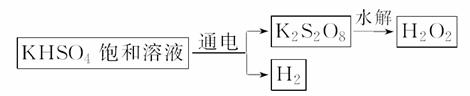
现用此法制取一定浓度的H2O2,并测定H2O2的质量分数。
已知:2MnO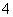 +5H2O2+6H+===2Mn2++8H2O+5O2↑
+5H2O2+6H+===2Mn2++8H2O+5O2↑
①取10.00 mL H2O2溶液(密度为1.00 g·mL-1)置于锥形瓶中加水稀释,并加稀硫酸酸化;
②用0.200 0 mol·L-1KMnO4溶液滴定;
③用同样方法滴定四次,消耗KMnO4溶液的体积分别为:40.00 mL、39.98 mL、42.02 mL、40.02 mL。
(4)用该原理制取H2O2的阳极电极反应式为_______________________________。
(5)进行操作②时,滴入第一滴KMnO4溶液,溶液的紫红色消失很慢,随着滴定的进行,溶液的紫红色消失速率加快,推测其原因可能是_____________________________。
(6)此H2O2溶液中溶质的质量分数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化合物中,含有非极性共价键的离子化合物是( )
A.CaC2 B.N2H4
C.Na2S2 D.NH4NO3
Ⅱ. [2013·海南卷] (14分)
图(a)所示的转化关系中(具体反应条件略),a、b、c和d分别为四种短周期元素的常见单质,其余均为它们的化合物,i的溶液为常见的酸。a的一种同素异形体的晶胞如图(b)所示。
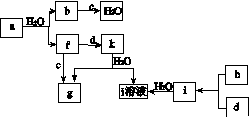
(a)

(b)
回答下列问题:
(1)图(b)对应的物质名称是________,其晶胞中的原子数为________,晶体的类型为________。
(2)d中元素的原子核外电子排布式为____________。
(3)图(a)中由二种元素组成的物质中,沸点最高的是________,原因是____________________,该物质的分子构型为________,中心原子的杂化轨道类型为________。
(4)图(a)中的双原子分子中,极性最大的分子是________。
(5)k的分子式为________,中心原子的杂化轨道类型为________,属于________分子(填“极性”或“非极性”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)、下列3种不同粒子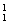 H、
H、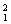 H、
H、 H表示______种元素,______种核素,
H表示______种元素,______种核素,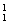 H、
H、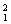 H、
H、 H互称为__________________。
H互称为__________________。
(2)下列各组物质中,互称为同分异构体的是( )
A.水与冰 B.O2与O3
C.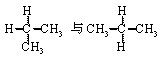 D.
D.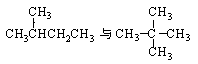
(3)写出电子式:(1)OH—: ;(2)N2: ;(3)K2O: ;(4)CO2: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组的同学们按照下面的实验方法制备氢氧化铁胶体:首先取少量蒸馏水于洁净的烧杯中,用酒精灯加热至沸腾,向烧杯中逐滴滴加饱和的FeCl3溶液继续煮沸,至液体呈透明的红褐色。
FeCl3+3H2O Fe(OH)3(胶体)+3HCl
Fe(OH)3(胶体)+3HCl
(1)判断胶体制备是否成功,可利用胶体的____________________。
(2)在做制备氢氧化铁胶体的实验时,有些同学没有按要求进行,结果没有观察到胶体,请你预测其现象并分析原因:
①甲同学没有选用饱和氯化铁溶液,而是将稀氯化铁溶液滴入沸水中,结果没有观察到________________,其原因是______________________________________________________________。
②乙同学在实验中没有使用蒸馏水,而是用自来水,结果会________________,原因是__________________________________________
____________________________________________________。
③丙同学向沸水中滴加饱和氯化铁溶液后,长时间加热,结果会_______ _________,原因是_________________________________________
_________,原因是_________________________________________
_______________________________________________________。
(3)丁同学按要求制备了Fe(OH)3胶体,但是他又向Fe(OH)3胶体中逐滴加入了稀H2SO4溶液,结果出现了一系列变化。
①先出现红褐色沉淀,原因是___________________________________
________________________________________________________。
②随后沉淀溶解,此反应的离子方程式为_________________________
__________________________ ________________________________。
________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
全球核安全峰会在华盛顿举行,发展核电、制裁核武器发展是会议主题。各式各样电池的发展是化学对人类的一项重大贡献。下列有关电池的叙述正确的是
( )
A.手机上用的锂离子电池属于一次电池
B.锌锰干电池中,锌电极是负极
C.氢氧燃料电池工作时氢气在负极被还原
D.太阳能电池的主要材料为二氧化硅
查看答案和解析>>
科目:高中化学 来源: 题型:
已知电极上每通过96 500 C的电量就会有1 mol电子发生转移。精确测量金属离子在惰性电极上以镀层形式沉积的金属质量,可以确定电解过程中通过电解池的电量。实际测量中,常用银电量计,如图所示。下列说法不正确的是

A.电量计中的银棒应与电源的正极相连,铂坩埚上发生的电极反应是:Ag++e-= Ag
B.称量电解前后铂坩埚的质量变化,得金属银的沉积量为108.0 mg,则电解过程中通过电解池的电量为96.5 C
C.实验中,为了避免银溶解过程中可能产生的金属颗粒掉进铂坩埚而导致测量误差,常在银电极附近增加一个收集网袋。若没有收集网袋,测量结果会偏高。
D.若要测定电解饱和食盐水时通过的电量,可将该银电量计中的银棒与待测电解池的阳极相连,铂坩埚与电源的负极相连。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com