
下列有关实验仪器的使用及实验操作正确的是
A. 加热蒸发皿和烧杯必须垫石棉网
B. 除去乙醇中的乙酸,加入NaOH溶液后分液
C. 将硫酸铜溶液蒸发浓缩、冷却结晶得到CuSO4·5H2O
D. 配制1L0.1mol·L-1NaCl溶液的实验中,用托盘天平称取5.85gNaCl
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016-2017学年河南省南阳市高一下学期第一次月考(3月)化学试卷(解析版) 题型:选择题
同一周期的X、Y、Z三种元素,已知最高价氧化物对应水化物的酸性顺序为HXO4>H2YO4>H3ZO4,则下列判断错误的是
A. 原子半径:X>Y>Z B. 气态氢化物的稳定性:HX>H2Y>ZH3
C. 元素原子得电子能力:X>Y>Z D. 阴离子的还原性:Z3->Y2->X-
查看答案和解析>>
科目:高中化学 来源:2017届全国新课程高考仿真信息理综(一)化学试卷(解析版) 题型:简答题
化学反应原理在工业生产中有广泛的应用。
(1)工业合成氨气的氢气主要来自天然气与水的反应, 但这种原料气中含有CO杂质,工业生产中通过下列反应来实现原料气中CO的除去。
CO(g)+H2O(g) CO(g)+ H2(g) △H<0。一定条件下反应达到平衡后采取_____措施可提高CO的转化率。在容积为2L的容器中发生上述反应,其中c(CO2)与反应时间(t)的关系如图甲所示,在t0时刻将容器体积扩大至4L,在图甲中画出t0时刻后。c(CO2)与反应时间(t)的变化曲线_____。
CO(g)+ H2(g) △H<0。一定条件下反应达到平衡后采取_____措施可提高CO的转化率。在容积为2L的容器中发生上述反应,其中c(CO2)与反应时间(t)的关系如图甲所示,在t0时刻将容器体积扩大至4L,在图甲中画出t0时刻后。c(CO2)与反应时间(t)的变化曲线_____。

(2)氨气的重要用途是合成尿素. 当加料比n(NH3)/n(CO2)=4时,CO2的转化率变化如图乙所示,a点v(CO2)逆______点v(CO2)正(填“大于”、“小于”或“等于”)。NH3的平衡转化率是______。
(3)某科研小组利用CO和H2在密闭容器中反应合成甲醇的实验,容器的开始体积是VL,实验中向容器中加人CO nmol, H22nmol,在一定的压强和催化剂的作用下反应:CO (g)+ 2H2(g) CH3OH(g)。右图为反应达到平衡时CO的转化率与温度、压强的关系。回答下列问题。
CH3OH(g)。右图为反应达到平衡时CO的转化率与温度、压强的关系。回答下列问题。

①上述合成甲醇的反应是______(填 “吸热”或“放热”)反应,图像中的压强p1、p2、p3的大小关系是_______。
②由图像分析压强p1温度是100℃时合成甲醇反应的平衡常数K=_______。
③在压强是p1温度是100℃的条件下,开始若向容器中加入CO 2nmol,H24nmol,反应达到平衡时CO的转化率_____(填“变大”、“变小”或“不变”),平衡时CO的物质的量_____(填“大于”、“小于”或“等于”)nmol
查看答案和解析>>
科目:高中化学 来源:安徽省皖北协作区2017届高三第19届(3月)联考理综化学试卷 题型:选择题
下列实验的现象以及结论均正确的是
选项 | 实验 | 现象 | 结论 |
A | 将少量的氯水滴入FeBr2溶液中,再滴 加CCl4振荡 | 下层溶液呈橙红色 | 还原性:Br->Fe2+ |
B | 向某无色溶液中滴加稀盐酸酸化的BaCl2溶液 | 产生白色沉淀 | 该溶液中一定存在SO42- |
C | 某钾盐溶于盐酸,将产生的无色无味气体通入澄清石灰水 | 石灰水变浑浊 | 该钾盐是K2CO3 |
D | 在两只试管中各加入2 mL5%H2O2浓溶液,向其中一只试管中滴入2滴0.1mol/LFeCl3溶液 | 加FeCl3溶液的试管中产生的气泡快 | 催化剂能增大化学反应速率 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源:2017届高考信息卷(全国卷I)理科综合(一)化学试卷(解析版) 题型:填空题
甲醇是重要的化学工业基础原料和清洁液体燃料。工业上可利用CO或CO2来生产燃料甲醇。已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
化学反应 | 平衡常数 | 温度 | |
500 | 800 | ||
①2H2(g)+CO(g) | K1 | 2.5 | 0.15 |
②H2(g)+CO2(g) | K2 | 1.00 | 2.5 |
③3H2(g)+CO2(g) | K3 | ||
(1)在体积一定的密闭容器中发生反应②,达到平衡后升高温度,下列说法正确的是____________
A.平衡正向移动 B.达到新的平衡后体系的压强增大
C.H2的转化率增大 D.体系的密度增大
(2)某温度下反应①中H2的平衡转化率(α)与体系总压强(p)的关系如图所示,若开始加入2molH2和1molCO,A点时容器的体积为1L,则B点的化学平衡常数为_______。

(3)据反应①与②可推导出Kl、K2与K3之间的关系,则K3=__________。(用K1、K2表示)。500℃时测得反应③在某时刻,H2(g)、CO2(g)、CH3OH(g)、H2O(g) 的浓度(mol/L)分别为0.8、0.1、0.3、0.15,则此时v正_______ v逆(填“> ”、“= ”或“< ")。
(4)在3L容积可变的密闭容器中发生反应②,已知c(CO)一反应时间t变化曲线l如图所示,若在t0时刻分别改变一个条件,曲线I变为曲线II和曲线III。

当曲线I变为曲线II时,改变的条件可能是________。当曲线I变为曲线III时,改变的条件可能是___________。
(5)一定条件下甲醇与一氧化碳反应可以合成乙酸。通常状况下,将a mol/L的醋酸与bmol/LBa (OH)2溶液等体积混合,反应平衡时,2c(Ba2+)=c(CH3COO-),用含a和b的代数式表示该混合溶液中醋酸的电离常数为_______。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省邯郸市高一3月月考化学试卷(解析版) 题型:推断题
有关物质间有如图所示的转化关系。已知B、D、G是常见的金属单质,E为常见的非金属单质,H常温下为无色液体,K为红棕色气体。
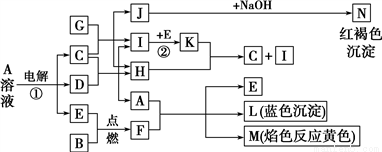
(1)F的电子式为______________,写出其与CO2反应的化学方程式并用双线桥标出电子转移的方向和数目:_________________________________
(2)反应①的离子方程式为____________________________________________。
(3)C与足量G反应的化学方程式为_____________________________________。其中,还原剂与氧化剂的物质的量之比为____________,检验反应中生成的金属离子的试剂为______________。
(4)Al能与A发生置换反应,生成物溶质与Na2CO3不能在溶液中大量共存,用离子方程式表示其原因:__________________________________
(5)I可由某种氢化物催化氧化得到,其反应的化学方程式为_______________________________。
(6)漂白粉和F都应密封保存,写出漂白粉露置于空气中失效的化学方程式:________________________________________________________________________
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省邯郸市高一3月月考化学试卷(解析版) 题型:选择题
根据表中提供的部分短周期元素原子半径及主要化合价的信息,判断以下叙述中正确的是( )
元素代号 | L | M | Q | R | T |
原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
A. 氢化物的沸点为H2T<H2R
B. 单质与稀盐酸反应的速率为L<Q
C. M与T形成的化合物具有两性
D. L2+与R2-的核外电子数相等
查看答案和解析>>
科目:高中化学 来源:2017届江苏省南通市高三高考全真模拟(三)化学试卷(解析版) 题型:填空题
【选修3:物质结构与性质】某钙钛型复合氧化物(如图),以A原子为晶胞的顶点,A位可以是Ca、Sr、Ba或Pb,当B位是V、Cr、Mn、Fe时,这种化合物的电阻率在有外磁场作用时较之无外磁场作用时存在巨大变化(巨磁电阻效应)。

(1)用A、B、O表示这类特殊晶体的化学式 。在图中,与A原子配位的氧原子数目为 。
(2)基态Cr原子的核外电子排布式为 ,其中电子的运动状态有 种。
(3)某些钙钛型复合氧化物能够催化NO直接分解为N2和O2,N和O的基态原子中,未成对的电子数目比为 。
(4)下表是几种碳酸盐的热分解温度和阳离子半径
碳酸盐 | CaCO3 | SrCO3 | BaCO3 |
热分解温度/℃ | 900 | 1172 | 1360 |
阳离子半径/pm | 99 | 112 | 135 |
请解释碳酸钙热分解温度最低的原因:_____________。
(5)用晶体的X射线衍射法可以测得阿伏伽德罗常数。对金属钙的测定得到以下结果:晶胞为面心立方最密堆积,边长为a pm,阿伏加德罗常数的值为NA,金属钙的密度为 g·cm-3(用含a和NA的式子表示)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省邯郸市高二3月月考化学试卷(解析版) 题型:选择题
有下述有机反应类型:①消去反应 ②水解反应 ③加聚反应 ④加成反应 ⑤还原反应 ⑥氧化反应。以丙醛为原料制取1,2?丙二醇,所需进行的反应类型依次是( )
A.⑥④②① B.⑤①④② C.①③②⑤ D.⑤②④①
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com