
【题目】在实验室可以用如图所示的装置制取乙酸乙酯,请回答下列问题.

(1)乙醇分子中官能团的名称是__________.
(2)试管a中发生反应的化学方程式为________________ 。
(3)浓H2SO4的作用是:_______________.(只写一种)
(4)反应开始前,试管b中盛放的溶液是___________________.
【答案】 羟基 CH3CH2OH+CH3COOH![]() CH3COOC2H5+H2O 催化剂或吸水剂 饱和碳酸钠溶液
CH3COOC2H5+H2O 催化剂或吸水剂 饱和碳酸钠溶液
【解析】试题分析:(1)乙醇分子的结构简式是CH3CH2OH,官能团是-OH;
(2)试管a中乙醇、乙酸在浓硫酸作用下生成乙酸乙酯。
(3)乙酸与乙醇发生酯化反应,需浓硫酸作催化剂,该反应为可逆反应,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动;
(4)制备乙酸乙酯时常用饱和碳酸钠溶液吸收乙酸乙酯,目的是除去乙醇和乙酸,便于闻乙酸乙酯的香味,降低乙酸乙酯的溶解度,便于分层。
解析:根据以上分析,(1)乙醇分子中官能团是-OH,名称是羟基。
(2)乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,该反应为可逆反应为:CH3CH2OH+CH3COOH![]() CH3COOC2H5+H2O。
CH3COOC2H5+H2O。
(3)乙酸与乙醇发生酯化反应,需浓硫酸作催化剂,该反应为可逆反应,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动,浓硫酸的作用为催化剂,吸水剂
(4)反应开始前,试管b中盛放的溶液是饱和碳酸钠溶液。


 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案 互动课堂系列答案
互动课堂系列答案科目:高中化学 来源: 题型:
【题目】已知卤代烃可以和钠发生反应,例如溴乙烷与钠发生反应为:2CH3CH2Br + 2Na![]() CH3CH2CH2CH3 + 2NaBr,应用这一反应,下列所给化合物中可以与钠合成环丁烷的是( )
CH3CH2CH2CH3 + 2NaBr,应用这一反应,下列所给化合物中可以与钠合成环丁烷的是( )
A. CH2BrCH2CH2CH2Br B. CH3CH2CH2CH2Br
C. CH3CHBrCHBrCH3 D. CH3Br
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去下列物质中的杂质(括号内是杂质)所用试剂不正确的是( )
A. NaHCO3溶液[Na2CO3]:用CO2气体 B. Mg粉[Al]:用NaOH溶液
C. CO2气体[H2O]:用碱石灰 D. HNO3溶液[HCl]:用AgNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中可以获得淡水、食盐,并可提取镁和溴等物质。
(1)海水淡化的方法有_______(填一种)。
(2)写出氯化钠的形成过程:_____________。
(3)从海水中提取镁的流程如下图所示:
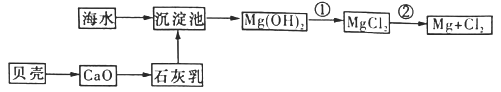
反应②的化学方程式为_______________。
从海水中提取溴的主要步骤是向浓缩的海水中通人氯气,将溴离子氧化,该反应的离子方程式为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将10mL单质气体X2和20mL单质气体Y2完全反应后,恰好生成20mL气体Z,若上述三种气体的体积都是在同温、同压下测定的,则气体Z的分子式是( )
A. XY2 B. X2Y C. XY D. X2Y4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可用甲烷和氧气按9:1的体积比混合,在200℃和10MPa的条件下,通过铜制管道反应制得甲醇:2CH4+O2=2CH3COH。
(1)已知一定条件下,CH4和CH3COH燃烧的热化学方程式分别为:
CH4(g)+SO2(g)=CO2(g)+2H2(g) △H=-802kJ/lmol
CH3OH(g)+l.5O2(g)=CO2(g)+2H2O(g) △H=-677kJ/mol
则2CH4(g)+O2(g)=2CH3OH(g) △H=__________
(2)甲烷固体氧化物燃料电池属于第三代燃料电池,是一种在中高温下直接将储存在燃料和氧化剂中的化学能高效、环境友好地转化成电能的全固态化学发电装置。其工作原理如下图所示。a是电池的____极(填“正”或“负”) ,b极的电极反应式为__________。

(3)工业上合成甲醇的另一种方法为:
CO(g)+2H2(g) ![]() CH3OH(g) △H=-90kJ/mol
CH3OH(g) △H=-90kJ/mol
T℃时,将2mol CO 和4molH2充入1L 的密闭容器中,测得H2的物质的量随时间变化如下图实线所示。
① 能用于判断反应已达化学平衡状态的是____________。
A.气体的总压强不再改变
B. H2与CH3OH的体积比不再改变
C.气体的密度不再改变
D.单位时间内消耗1mol CO,同时生成1mol CH3OH
② 请计算出T℃ 时反应的平衡常数K=_________________。
③ 仅改变某一实验条件再进行两次实验测得H2的物质的量随时间变化如图中虚线所示。曲线Ⅰ对应的实验条件改变是:________;曲线Ⅱ对应的实验条件改变是_________0。

④ a、b、c三点逆反应速率由大到小排列的顺序是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物X是一种医药中间体,其结构简式如图所示。

下列有关化合物X的说法正确的是
A. 分子中两个苯环一定处于同一平面
B. 不能与饱和Na2CO3溶液反应
C. 1 mol化合物X最多能与2 molNaOH反应
D. 在酸性条件下水解,水解产物只有一种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、M的原子序数依次增大,元素X的一种高硬度单质是宝石,Y2+电子层结构与氖相同,Z的质子数为偶数,室温下M单质为淡黄色固体,回答下列问题:
(1)M元素在周期表中的位置______________________________。
(2)Z元素在自然界中常见的二元化合物是_______,其与NaOH溶液反应的离子方程式为___________________________________________。
(3)X与M的单质能在高温下反应,生成产物的分子结构与CO2相似,请写出该产物分子的电子式_______________,其化学键属__________共价键(填“极性”或“非极性”)。
(4)四种元素中的____可用于航空航天合金材料的制备,其单质与X的一种氧化物反应的化学方程式为 _______________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com