
科目:高中化学 来源: 题型:
| A、2.4gMg与足量的盐酸反应失去的电子数为0.2NA |
| B、11.2L氯气所含的分子数为0.5NA |
| C、32g氧气中所含的氧原子数为NA |
| D、18g水中所含的电子数为8NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | E | F |
查看答案和解析>>
科目:高中化学 来源: 题型:
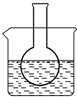 三个课外实验小组用Na2SO3溶液、FeCl3溶液及其它试剂做了一系列实验:
三个课外实验小组用Na2SO3溶液、FeCl3溶液及其它试剂做了一系列实验:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用Na2CO3溶液不能区分CH3COOH和CH3COOCH2CH3 |
| B、将碘酒滴在鸡蛋清中,可观察到鸡蛋清显蓝色 |
| C、乙酸的酯化反应和苯的硝化反应属于同种反应类型 |
| D、乙烯能够发生加成反应,结构简式为CH2CH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
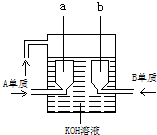 A、B、C、D4种短周期元素的原子序数依次增大,其中A、C及B、D分别是同主族元素,又知两元素的质子数之和B、D是A、C的2倍,这4种元素的单质中有2种是气体,2种是固体.
A、B、C、D4种短周期元素的原子序数依次增大,其中A、C及B、D分别是同主族元素,又知两元素的质子数之和B、D是A、C的2倍,这4种元素的单质中有2种是气体,2种是固体.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com