
����Ŀ����ʽ�Ȼ�þ(MgOHCl)�������������Ӽ�����ҵ���Ʊ������϶࣬��������������þ�ȷֽ��Ȼ���ư������õ���ʽ�Ȼ�þ�Ĺ��������ҹ��״���ij��ѧ����С����ݸ�ԭ���������װ��ͼ�������ʵ�飬װ��C��CuO������Ϊ8.0 g��

��ش��������⣺
��1��װ��A�з�����Ӧ���ɼ�ʽ�Ȼ�þ�Ļ�ѧ����ʽΪ��_____________________________��
��2��װ��D�����ɳ�����������Ӧ�����ӷ���ʽΪ_________________________________��
��3����Ӧ�����г���ͨ��N2�����������㣺һ��: ��װ��A�в����İ�����ȫ����������:_______________________________��
��4������ü�ʯ�ҵ�����������a g����õ���ʽ�Ȼ�þ������Ϊ_______g��
��5����Ӧ��ϣ�װ��C�е�����ͭȫ���ɺ�ɫ��Ϊ��ɫ����������Ϊ6.8 g�������ɵ������ֱ���ŷŵ������У����ɫ������_______���÷�Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ_______mol��
��6���������һ��ʵ�鷽��֤��װ��C�е�����ͭ��Ӧ��ȫ��õ��ĺ�ɫ�����к���������ͭ����֪����Cu2O��2H��===Cu2����Cu��H2O
����ѡ�Լ���2 mol��L��1H2SO4��Һ��Ũ���ᡢ2 mol��L��1HNO3��Һ��10 mol��L��1 HNO3��Һ
ʵ�鲽�� | Ԥ������ͽ��� |
����1��ȡ��Ӧ��װ��C�е������������Թ��� | |
����2��____________ | ____________ |
���𰸡�Mg(OH)2��NH4Cl![]() MgOHCl��NH3����H2O Al3����3NH3��H2O=Al(OH)3����3NH ϡ�Ͱ�������ֹ���� 4.25a Cu��Cu2O 0.15 ���Թ��м�������2 mol��L��1H2SO4��Һ ��Һ�����ɫ��˵����ɫ�����к���Cu2O
MgOHCl��NH3����H2O Al3����3NH3��H2O=Al(OH)3����3NH ϡ�Ͱ�������ֹ���� 4.25a Cu��Cu2O 0.15 ���Թ��м�������2 mol��L��1H2SO4��Һ ��Һ�����ɫ��˵����ɫ�����к���Cu2O
��������
A�з�Ӧ�õ�MgOHCl��������NH3��H2O����ʯ�Ҹ��ﰱ����C�а���������ͭ��Ӧ��õ�������ˮ��D���������ˮ��Ӧ����������D�а���������������������F��NO��������Ӧ�õ�����������G�ж��������ܽ�õ����ᣬ������Cu��Ӧ���ݴ˷������
(1)A��������þ���Ȼ���ټ��������·�Ӧ����MgOHCl��NH3��H2O����Ӧ����ʽΪ��Mg(OH)2+NH4Cl ![]() MgOHCl+NH3��+H2O���ʴ�Ϊ��Mg(OH)2+NH4Cl
MgOHCl+NH3��+H2O���ʴ�Ϊ��Mg(OH)2+NH4Cl ![]() MgOHCl+NH3��+H2O��
MgOHCl+NH3��+H2O��
(2)��ˮ���Ȼ�����Ӧ�����Ȼ�狀�������������Ӧ�����ӷ���ʽΪAl3++3NH3H2O=Al(OH)3��+3NH4+���ʴ�Ϊ��Al3++3NH3H2O=Al(OH)3��+3NH4+��
(3)G�ж���������������������ˮ���ܽ�ᵼ�µ�����ͨ�뵪������ϡ�Ͱ�������ֹ�������ʴ�Ϊ��ϡ�Ͱ�������ֹ������
(4)����ü�ʯ�ҵ�����������a g�������ɵ�ˮ������Ϊag������Mg(OH)2+NH4Cl ![]() MgOHCl+NH3��+H2O�����ɵļ�ʽ�Ȼ�þ������Ϊ
MgOHCl+NH3��+H2O�����ɵļ�ʽ�Ȼ�þ������Ϊ![]() ��76.5g/mol=4.25a g���ʴ�Ϊ��4.25a��
��76.5g/mol=4.25a g���ʴ�Ϊ��4.25a��
(5)��ɫ����ΪCu��Cu2O�����������������������Ϊ���ٵ���Ԫ������������ٵ���Ԫ������Ϊ8g-6.8g=1.2g����CuO����Ԫ������Ϊ8.0g�� ![]() =1.6g��1.2g���ʺ�ɫ����ΪCu��Cu2O������������ʵ����ֱ�Ϊxmol��ymol����x+2y��
=1.6g��1.2g���ʺ�ɫ����ΪCu��Cu2O������������ʵ����ֱ�Ϊxmol��ymol����x+2y��![]() ��64x+144y�����x=0.05��y=0.025����ת�Ƶ���Ϊ0.05mol��2+0.025mol��2=0.15mol���ʴ�Ϊ��Cu��Cu2O��0.15��
��64x+144y�����x=0.05��y=0.025����ת�Ƶ���Ϊ0.05mol��2+0.025mol��2=0.15mol���ʴ�Ϊ��Cu��Cu2O��0.15��
(6)Cu����Ũ���ᷴӦ��Cu2O����ϡ�ᷴӦ�õ�Cu2+����ϡH2SO4��Һ�ܽ⣬��Һ�г�����ɫ��˵����ɫ�����к���Cu2O���ʴ�Ϊ�����Թ��м�������2 mol��L��1H2SO4��Һ����Һ�����ɫ��˵����ɫ�����к���Cu2O��


 ��ѧʵ����ϵ�д�
��ѧʵ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
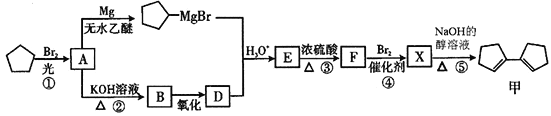
����Ŀ���л������������ȡ��Ĺ�Ч����ϳ�·�����£�
��֪��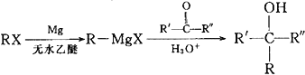 (R��R'��R"������������)
(R��R'��R"������������)
��1���л���ķ���ʽΪ___________���л���A�к��еĹ����ŵ�����Ϊ_______________��
��2���л���B��������__________����B��D ����ķ�Ӧ�Լ��ͷ�Ӧ����Ϊ________________��
��3����������~�ݷ�Ӧ�У�����ȡ����Ӧ����____________(�����)��
��4��д��E��F�Ļ�ѧ����ʽ________________��
��5�����������ڷ����廯�������ļ�ͬ���칹����________�֡����к˴Ź���������ֻ��2���Ľṹ��ʽ��______________
��6�����������Ϣ��д����CH4Ϊԭ���Ʊ�CH3CHO�ĺϳ�·�ߣ������Լ���ѡ��__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȼ�ŵ��̻������ˡ���ɫ��Ӧ����ԭ��������˵������ȷ���ǣ� ��
A.��ɫ��Ӧ���ڻ�ѧ�仯
B.NaCl��Na2CO3����ʱ������ɫ��ͬ
C.ij��Ʒ����ɫ��ɫΪ��ɫ�������Ʒ��������Ԫ��
D.��ɫ��Ӧʱ����˿Ӧ��������ϴ����������������û����ɫ����պȡ��Ʒ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ����ش��������⣺

��1������ԭ����У�a�缫�����ݲ�����b�缫��ϸ�����ԭ��ص�������___����д��ĸ��a����b���������·�е��������ķ�����___��b�缫�����ķ�Ӧ������____���������Ӧ����ԭ��Ӧ������
��2�����缫aΪZn���缫bΪAg���������ҺΪCuSO4ʱ��д����ԭ����ܵ����ӷ�Ӧ����ʽ��____�������ĵ缫��ӦʽΪ____����a���ܽ������Ϊ6.5gʱ����_____mol����ͨ�����ߡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1�������и������������գ�
�� O2��O3 �� �� 12C��13C��14C�� �� C2H6��C5H12�� ��C3H6��C5H10����14N��14C
�� ![]() ��
��![]() ���� CH3 (CH2) 3 CH3��
���� CH3 (CH2) 3 CH3��![]()
��Ϊͬλ�ص���______�� ��Ϊͬ�����������_______ �� ��Ϊͬϵ�����_______����Ϊͬ���칹�����_______ ������ͬһ���ʵ��� _______ ��
��2����ȥ�屽�е��壺�Լ��ǣ�________����Ӧ�Ļ�ѧ����ʽΪ____________________
��3��һ���������Ҵ�����������ʱȼ�գ��õ�CO��CO2��H20������Ϊ27.6g����H2O������Ϊ10.8g����CO2������Ϊ_____________g
��4��2g C2H2��ȫȼ������Һ̬ˮ��CO2���ų�99.6kJ��������C2H2ȼ���ȵ��Ȼ�ѧ����ʽ��_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������У�����������һ����ͬ����(����)
A. 10 g H2��10 g O2 B. 5.6 L N2��5.6 L CO2
C. 14 g CO��0.5 mol Br2 D. ��״����2.24 L H2O��0.1 mol N2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں��¡����������£���˵�����淴Ӧ��H2(g)+I2(g)![]() 2HI(g)�ﵽƽ��״̬����
2HI(g)�ﵽƽ��״̬����
A. v(H2)��=2v(HI)��B. �������ɫ���ֲ���
C. ������ܶȱ��ֲ���D. �����ѹǿ���ֲ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и���������ָ����Һ��һ���ܴ����������
A. ��ʹ���ȱ�����Һ��Na����NH4����NO3����CO32��
B. ���뱽������ɫ����Һ��K����NH4����Cl����SCN��
C. �����£�![]() ��1��10��14����Һ��K����Na����AlO2����CO32��
��1��10��14����Һ��K����Na����AlO2����CO32��
D. ����Al�ܷų�����H2����Һ��Na����Fe2����NO3����SO42��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NOx����ҪָNO��NO2���Ǵ�����Ҫ��Ⱦ��֮һ����Чȥ�������е�NOx�ǻ�����������Ҫ���⡣
��1����ˮ����NOx������Ȼ�ѧ����ʽ���£�
2NO2��g��+H2O��l��![]() HNO3��aq��+HNO2��aq�� ��H=116.1 kJ��mol1
HNO3��aq��+HNO2��aq�� ��H=116.1 kJ��mol1
3HNO2��aq��![]() HNO3��aq��+2NO��g��+H2O��l�� ��H=75.9 kJ��mol1
HNO3��aq��+2NO��g��+H2O��l�� ��H=75.9 kJ��mol1
��Ӧ3NO2��g��+H2O��l��![]() 2HNO3��aq��+NO��g������H=___________kJ��mol1��
2HNO3��aq��+NO��g������H=___________kJ��mol1��
��2����ϡ��������NOx���õ�HNO3��HNO2�Ļ����Һ�����û����Һ�ɻ�ý�Ũ�����ᡣд�����ʱ�����ĵ缫��Ӧʽ��____________________________________��
��3��������(NH2)2COˮ��Һ����NOx�����չ����д���HNO2��(NH2)2CO����N2��CO2�ķ�Ӧ��д���÷�Ӧ�Ļ�ѧ����ʽ��____________________________________��
��4�������������£����ʹ���M�ܴ�NH3��NOx��Ӧ����N2��
��NH3��NO2����N2�ķ�Ӧ�У�������1 mol N2ʱ��ת�Ƶĵ�����Ϊ__________mol��
�ڽ�һ��������O2��NH3��NOx�Ļ�����壬����ͨ��װ�д���M�ķ�Ӧ���з�Ӧ��װ�ü���20ͼ1����

��Ӧ��ͬʱ��NOx��ȥ�����淴Ӧ�¶ȵı仯��������20ͼ2��ʾ����50��250 �淶Χ�������¶ȵ����ߣ�NOx��ȥ������Ѹ��������������������Ҫԭ����____________________________������Ӧ�¶ȸ���380 ��ʱ��NOx��ȥ����Ѹ���½���ԭ�������___________________________��

�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com