
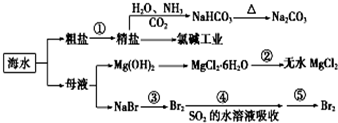
| A. | 过程①中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 | |
| B. | 工业上通过电解饱和MgCl2溶液制取金属镁 | |
| C. | 过程②中结晶出的MgCl2•6H2O要在HCl氛围中加热脱水制得无水MgCl2 | |
| D. | 在③④⑤步骤中,溴元素均被氧化 |
分析 海水晒盐得到粗盐和母液,粗盐除杂得到精盐,电解饱和食盐水得到氢氧化钠、氯气和氢气为氯碱工业,氨化的饱和食盐水中通入二氧化碳制备碳酸氢钠晶体,湿热分解生成碳酸钠,母液加入氢氧化钙沉淀镁离子生成氢氧化镁沉淀,过滤得到氢氧化镁沉淀溶解于盐酸得到氯化镁溶液浓缩蒸发结晶析出氯化镁晶体,在氯化氢气流中失水得到固体氯化镁,溴化钠溶液通入氯气生成溴单质,用二氧化硫吸收溴单质得到溴化氢,通过氯气氧化得到工业纯溴,
A.除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可以加过量的氯化钡除去硫酸根离子,然后用碳酸钠去除钙离子和过量的钡离子,盐酸要放在最后,来除去过量的氢氧化钠和碳酸钠,加氢氧化钠和氯化钡无先后顺序要求;选项中的试剂添加顺序中,钡离子最后无法除去;
B.工业上是电解熔融的氯化镁来制取金属镁;
C.氯化镁晶体脱水过程中镁离子易水解生成氢氧化镁沉淀,在氯化氢气体中脱水可以抑制镁离子水解;
D.第③步中,溴元素化合价从-1升高到0价,被氧化,第④步中,溴元素化合价从0降低到-1价,被还原,第⑤步中,溴元素化合价从-1升高到0价,被氧化;
解答 解:A.选项中的试剂添加顺序中,钡离子最后无法除去,则加入的药品顺序为:BaCl2溶液→NaOH溶液→Na2CO3溶液→过滤后加盐酸,故A错误;
B.工业上是电解熔融的氯化镁来制取金属镁,电解饱和MgCl2溶液得到的是氢氧化镁,故B错误.
C.氯化镁晶体脱水过程中镁离子易水解生成氢氧化镁沉淀,在氯化氢气体中脱水可以抑制镁离子水解;MgCl2•6H20要在HCl氛围中加热脱水制得无水MgCl2,故C正确;
D.依据转化关系的流程中,③步反应为:2NaBr+Cl2=Br2+2NaCl;④是Br2+SO2+2H2O=H2SO4+2HBr,⑤步的反应为:2HBr+Cl2=Br2+HCl;所以在过程③⑤中溴元素均被氧化,④中溴元素被还原,故D错误;故选C.
点评 本题考查了海水资源的综合应用,涉及物质的分离提纯等知识,侧重于化学与生活的综合运用,培养了学生运用知识分析问题的能力.难点是除杂过程中加入药品的先后顺序,要根据物质的特点来分析解答,题目难度中等.


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:选择题
| A. | 共价键一定存在于共价化合物中,也可能存在于离子化合物中 | |
| B. | Na2O2中既含有离子键也含有极性共价键 | |
| C. | NH4Cl是都由非金属元素组成的既含有离子键也含有共价键的离子化合物 | |
| D. | 熔化状态下不导电的化合物一定是共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (1)(2)(3)(4) | B. | (1)(2)(3)(4)(5) | C. | (1)(2)(4) | D. | (1)(2)(4)(5) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6.02×1023就是阿伏加德罗常数 | |
| B. | 1mol Cl2含有2NA个氯原子 | |
| C. | 摩尔既可表示质量,又可以表示数量 | |
| D. | 32g O2所含O2的摩尔数是1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
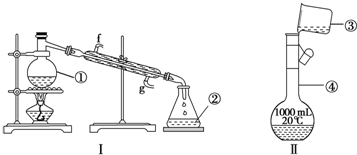
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
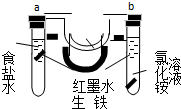 如图装置中,U型管内为红墨水,a、b试管中分别盛有食盐水和氯化铵溶液,各加入生铁块,放置一段时间.下列有关描述错误的是( )
如图装置中,U型管内为红墨水,a、b试管中分别盛有食盐水和氯化铵溶液,各加入生铁块,放置一段时间.下列有关描述错误的是( )| A. | a中发生了吸氧腐蚀,b中发生了析氢腐蚀 | |
| B. | 两试管中负极反应均是:Fe-2e-=Fe2+ | |
| C. | 生铁块中碳作原电池正极 | |
| D. | 红墨水在一段时间后,两边液面变为左低右高 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | O4的摩尔质量是64 | B. | O2、O3、O4都是氧的同位素 | ||
| C. | O2、O3、O4都是氧的同素异形体 | D. | O2、O3、O4互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间/浓度 | C(NH3)(mol•L-1) | C(O2)(mol•L-1) | C(NO)(mol•L-1) |
| 起始 | 0.8000 | 1.600 | 0.000 |
| 第2min | 0.6000 | a | 0.2000 |
| 第4min | 0.3000 | 0.9750 | 0.5000 |
| 第6min | 0.3000 | 0.9750 | 0.5000 |
| 第8min | 0.7000 | 1.475 | 0.1000 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com