
【题目】把1.0mol/L CuSO4溶液、1.0mol/L Fe2(SO4)3溶液两种溶液等体积混合(假设混合后液体的体积等于混合前两种溶液的体积之和),向溶液中加入足量铁粉,经足够长的时间后,铁粉有剩余.此时溶液中Fe2+的物质的量浓度为( )
A.1.0 mol/L
B.2.0 mol/L
C.3.0 mol/L
D.4.0 mol/L
【答案】B
【解析】把1.0mol/LCuSO4和1.0mol/L Fe2(SO4)3溶液等体积混合,稀释前后溶质的物质的量不变,则混合后溶液中c(CuSO4)= ![]() ×1.0mol/L=0.5mol/L,c(H2SO4)=
×1.0mol/L=0.5mol/L,c(H2SO4)= ![]() ×1.0mol/L=0.5mol/L,混合后溶液中硫酸根来源于硫酸铜与硫酸铁电离,故 c(SO42﹣)=c(CuSO4)+3c[Fe2(SO4)3]=0.5mol/L+3×0.5mol/L=2mol/L,向溶液中加入铁粉,经过足够长的时间,铁粉有剩余,则硫酸铜、硫酸都完全反应,此时溶液中溶质为FeSO4 , 故c(Fe2+)=c(SO42﹣)=2mol/L.
×1.0mol/L=0.5mol/L,混合后溶液中硫酸根来源于硫酸铜与硫酸铁电离,故 c(SO42﹣)=c(CuSO4)+3c[Fe2(SO4)3]=0.5mol/L+3×0.5mol/L=2mol/L,向溶液中加入铁粉,经过足够长的时间,铁粉有剩余,则硫酸铜、硫酸都完全反应,此时溶液中溶质为FeSO4 , 故c(Fe2+)=c(SO42﹣)=2mol/L.
所以答案是:B


科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁、戊五种物质是中学化学常见的物质,其中甲、乙均为单质,它们的转化关系如图所示(某些条件和部分产物已略去).下列说法正确的是( ) 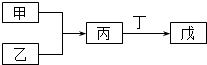
A.若甲可以与NaOH溶液反应放出H2 , 则丙一定是两性氧化物
B.若甲为短周期中最活泼的金属,且戊为碱,则丙生成戊一定是氧化还原反应
C.若丙、丁混合产生大量白烟,则乙可能具有漂白性
D.若甲、丙、戊都含有同一种元素,则三种物质中,该元素的化合价由低到高的顺序可能为甲<丙<戊
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道科研人员应用计算机模拟出结构类似C60的物质N60。已知:①N60分子中每个氮原子均以N—N键结合三个N原子而形成8电子稳定结构;②N—N键的键能为167kJ·mol-1。请回答下列问题:
(1)N60分子组成的晶体为晶体,其熔、沸点比N2(填“高”或“低”),原因是。
(2)1molN60分解成N2时吸收或放出的热量是kJ(已知N≡N键的键能为942kJ·mol-1),表明稳定性N60(填“>”“<”或“=”)N2。
(3)由(2)列举N60的用途(举一种):。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据氢气分子的形成过程示意图,回答问题。
氢气分子的形成过程示意图
(1)H—H键的键长为 , ①~⑤中,体系能量由高到低的顺序是。
(2)下列说法中正确的是 ( )
A.氢气分子中含有一个π键
B.由①到④,电子在核间出现的概率增大
C.由④到⑤,必须消耗外界的能量
D.氢气分子中含有一个极性共价键
(3)已知几种常见化学键的键能为
化学键 | Si—O | H—O | O O | Si—Si | Si—C |
460 | 467 | 498 | 176 | X |
请回答下列问题:
①比较Si—Si键与Si—C键的键能大小可知X(填“>”“ <”或“=”)176kJ·mol-1。
②H2被喻为21世纪人类最理想的燃料,而更有科学家提出硅是“21世纪的能源”“未来的石油”的观点。试计算:每千克H2燃烧(生成水蒸气)放出的热量约为;每摩尔硅完全燃烧放出的热量约为。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数由小到大排列的四种短周期元素X、Y、Z、W,其中X、Z、W与氢元素可组成共价化合物XH3、H2Z和HW;Y与氧元素可形成离子化合物Y2O和Y2O2。
(1)写出Y2O2的化学式: , 其中含有的化学键是。
(2)X、Z、W三种元素的最高价氧化物对应的水化物酸性最强的是(填写化学式)。
(3)XH3、H2Z和HW三种化合物中与另外两种都能反应的是(填写化学式),生成物属于(填“离子”或“共价”)化合物。
(4)写出下列物质的电子式:
①XW3:;
②Y2Z:。
(5)X的气态氢化物的结构式为。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.2 mol下列烃完全燃烧后,生成的气体缓缓通过0.5 L 2mol/L的NaOH溶液中,生成正盐和酸式盐的物质的量之比为1:3,则该烷烃是( )
A. 乙烷 B. 丙烷 C. 丁烷 D. 戊烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为有效控制雾霾,各地积极采取措施改善大气质量.有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要.
(1)在汽车排气管内安装催化转化器,可将汽车尾气中主要污染物转化为无毒的大气循环物质. 已知:①N2(g)+O2(g)═2NO(g)△H1=+180.5kJmol﹣1
②C和C0的燃烧热(△H)分别为﹣393.5kJmol﹣1和﹣283kJmol﹣1
则2NO(g)+2CO(g)═N2(g)+2CO2(g)的△H=kJmol﹣1
(2)将0.20mol NO和0.10mol CO充入一个容积为1L的密闭容器中,反应过程中物质浓度变化如图所示. ①CO在0﹣9min内的平均反应速率v(CO)=molL﹣1min﹣1(保留两位有效数字);第12min时改变的反应条件可能为 .
A.升高温度 B.加入NO C.加催化剂 D.降低温度
②该反应在第24min时达到平衡状态,CO2的体积分数为(保留三位有效数字),化学平衡常数K=(保留两位有效数字).
(3)烟气中的SO2可用某浓度NaOH溶液吸收得到Na2SO3和NaHSO3混合溶液,且所得溶液呈中性,该溶液中c(Na+)=(用含硫微粒浓度的代数式表示).
(4)通过人工光合作用能将水与燃煤产生的CO2转化成HCOOH和O2 . 已知常温下0.1molL﹣1的HCOONa溶液pH=10,则HCOOH的电离常数Ka= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图1所示,此装置可用来制取和观察Fe(OH)2在空气中被氧化时的颜色变化,实验时必须使用铁屑和6mol/L的硫酸,其他试剂任选.填写下列空白:
(1)B中盛有一定量的NaOH溶液,A中应预先加入试剂是 . A中反应的离子方程式是 .
(2)实验开始时应先将活塞a(填“打开”、“关闭”).
(3)简述生成Fe(OH)2的操作过程 .
(4)实验完毕,打开b处活塞,放入一部分空气,此时B瓶中发生的反应为 .
(5)下列图2各图示中能较长时间看到Fe(OH)2白色沉淀.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列烷烃在光照下与氯气反应,只生成一种一氯代烃的是( )
A. CH3CH2CH2CH3 B. CH3CH(CH3)2
C. CH3C(CH3)3 D. (CH3)2CHCH2CH3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com