
【题目】已知:I2在水中溶解度很小,在KI溶液中溶解度显著增大。 I2在KI溶液中存在下列平衡:I2(aq)+I-(aq) ![]() I3 -(aq)。测得不同温度下该反应的平衡常数如下图所示,下列说法正确的是( )
I3 -(aq)。测得不同温度下该反应的平衡常数如下图所示,下列说法正确的是( )
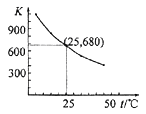
A.反应I2(aq)+I-(aq) ![]() I3 -(aq)的ΔH>0
I3 -(aq)的ΔH>0
B.利用该反应可以除去硫粉中少量的碘单质
C.在上述平衡体系中加入苯,平衡不移动
D.25℃时,在上述平衡体系中加入少量KI固体,平衡常数K小于680
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】乙烯是重要的化工原料,以乙烯为原料在不同条件下可合成下列物质(部分条件未标出):

(1)乙醇能与乙酸反应生成有果香味的物质,其名称为__________,该反应类型是____________
(2)反应⑥的化学方程式是______________实验现象是__________________
(3)反应③用KOH的乙醇溶液处理二氯乙烷制氯乙烯的方程式为:____________
(4)苯乙烯中所含官能团的名称_____________
(5)苯乙烯合成聚苯乙烯的化学方程式是_____________________
(6)以乙醇和苯乙烯为原料合成有机物![]() ,写出合成路线图_________________。
,写出合成路线图_________________。
(合成路线常用的表示方法为:![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】归纳法是高中化学学习常用的方法之一,某化学研究性学习小组在学习了《化学反应原理》后作出了如下的归纳总结,其中正确的是
①常温下,pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合,则有c (Na+) + c(H+)=c(OH-) + c(CH3COO-)
②对已建立化学平衡的某可逆反应,当改变条件使化学平衡向正反应方向移动时,生成物的百分含量一定增加
③常温下,AgCl在同物质的量浓度的CaCl2和NaCl溶液中的溶解度相同
④常温下,已知醋酸电离平衡常数为Ka;醋酸根水解平衡常数为Kh;水的离子积为Kw;则有:Ka·Kh=Kw
⑤电解精炼铜时,电解质溶液中铜离子浓度不变 。
A.①④ B.①②④ C.①②④⑤ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 用金属活动性顺序可解释反应:Na(l)+KCl(l)=NaCl(l)+K(g)
B. 水的电离是吸热过程,升高温度,水的离子积增大、pH减小
C. 对于平衡2HI(g)I2(g)+H2(g),压缩容器体积,平衡不移动,气体的颜色不变
D. 由反应SiO2+2C ![]() Si+2CO↑,可得出C的非金属性强于Si
Si+2CO↑,可得出C的非金属性强于Si
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项表述与示意图形不一致的是

A. 图①表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1NaOH溶液,溶液pH随加酸体积的变化
B. 图②中曲线表示反应2SO2(g) + O2(g)![]() 2SO3(g);ΔH < 0 正、逆反应的平衡常数K随温度的变化
2SO3(g);ΔH < 0 正、逆反应的平衡常数K随温度的变化
C. 图③表示10 mL 0.01 mol·L-1KMnO4酸性溶液与过量0.1 mol·L-1草酸溶液混合,n(Mn2+) 随时间的变化
D. 图④中a、b曲线分别表示反应CH2=CH2(g)+ H2(g) →CH3CH3(g);ΔH>0使用和未使用催化剂时,反应过程中的能量变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,PbO2与Cr3+反应,产物是Cr2O72-和Pb2+,则参加反应的Cr3+,与PbO2的个数之比
A. 2:3 B. 1:3 C. 1:1 D. 4:3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com