
(15分)二氧化碳是引起“温室效应”的主要物质,节能减排,高效利用能源,能够减少二氧化碳的排放。
(1)在一定温度下的2L固定容积的密闭容器中,通入2 molCO2和3mol H2,发生的反应为:CO2(g)+3H2(g) ? CH3OH(g)+H2O(g),△H=-a kJ·mol-1(a>0), 测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。

①能说明该反应已达平衡状态的是________。(选填编号)
A.CO2的体积分数在混合气体中保持不变
B.混合气体的平均相对分子质量不随时间的变化而变化
C.单位时间内每消耗1.2mol H2,同时生成0.4molH2O
D.该体系中H2O与CH3OH的物质的量浓度之比为1:1,且保持不变
②计算该温度下此反应的平衡常数K=_________。(保留两位有效数字)。若改变条件 (填选项),可使K=1。
A.增大压强
B.增大反应物浓度
C.降低温度
D.升高温度
E.加入催化剂
(2)某甲醇燃料电池原理如图1所示。

①M区发生反应的电极反应式为_______________________________。
②用上述电池做电源,用图2装置电解饱和食盐水(电极均为惰性电极),则该电解的总反应离子方程式为: 。假设溶液体积为300mL,当溶液的pH值变为13时(在常温下测定),理论上消耗甲醇的质量为______________(忽略溶液体积变化)。
(3)有一种用CO2生产甲醇燃料的方法:
已知:①CO2(g)+3H2(g)  CH3OH(g)+H2O(g) △H=-a kJ·mol-1;
CH3OH(g)+H2O(g) △H=-a kJ·mol-1;
②CH3OH(g)=CH3OH(l) △H=-b kJ·mol-1;
③2H2(g)+O2(g)=2H2O(g) △H=-c kJ·mol-1;
④H2O(g)=H2O(l) △H=-d kJ·mol-1,
则表示CH3OH(l)燃烧热的热化学方程式为:_____________________________
(15分)(1)①A、B(少选得1分,错选不得分) (2分) ②0.20 (2分) C (2分)
(2)①CH3OH-6e-+H2O=CO2+6H+(2分)
②2Cl-+2H2O H2↑+Cl2↑+2 OH-(2分) 0.16g(2分)
H2↑+Cl2↑+2 OH-(2分) 0.16g(2分)
CH3OH(l) +O2(g) =CO2(g) +2H2O(l) ΔH=-(c+2d-a-b)kJ/mol(3分)
【解析】
试题分析:(1)①A.若反应为达到平衡状态,则混合气体的物质的量就会发生变化,CO2的体积分数在混合气体中也会发生变化,若其保持不变,说明反应处于平衡状态,正确;B.该反应在反应前后气体的质量不变,而气体的物质的量发生变化,所以混合气体的平均相对分子质量不随时间的变化而变化,说明反应处于平衡状态,正确;C.在任何情况下都存在单位时间内每消耗1.2mol H2,同时生成0.4molH2O,所以不能确定反应是否处于平衡状态,错误;D.该体系中H2O与CH3OH都是生成物,它们的物质的量的比在任何情况下都是为1:1,因此不能确定反应是否处于平衡状态,错误。②根据图像既物质的开始浓度可知,在平衡时各种物质的浓度分别是:c(CO2)=0.75mol/L;c(H2)=0.75mol/L;c(CH3OH)=0.25mol/L;c(H2O)=0.25mol/L;所以在该温度下此反应的平衡常数K= =0.20;由于高反应的正反应是放热反应,如果平衡常数变为1,则平衡应该正向移动,由于化学平衡常数只与温度有关,而与其它条件无关,所以根据平衡移动原理可知应该降低反应的温度,因此选项是C;(2)由于阳离子的沸点能力:H+>Na+,所以H+在阴极放电,常数氢气,阴离子的沸点能力:Cl->OH-,因此Cl-在阳极放电产生氯气,用惰性电极电解饱和食盐水的总反应离子方程式是2Cl-+2H2O
=0.20;由于高反应的正反应是放热反应,如果平衡常数变为1,则平衡应该正向移动,由于化学平衡常数只与温度有关,而与其它条件无关,所以根据平衡移动原理可知应该降低反应的温度,因此选项是C;(2)由于阳离子的沸点能力:H+>Na+,所以H+在阴极放电,常数氢气,阴离子的沸点能力:Cl->OH-,因此Cl-在阳极放电产生氯气,用惰性电极电解饱和食盐水的总反应离子方程式是2Cl-+2H2O H2↑+Cl2↑+2 OH-;n(NaOH)=0.1mol/L×0.3L=0.03mol,n(e-)=0.03mol,在整个闭合回路中电子转移的数目相等,由于1mol的甲醇反应会失去6mol的电子,所以反应消耗的甲醇的物质的量是0.03mol÷6=0.005mol,甲醇的相对分子质量是32,所以小于消耗甲醇的质量是m(CH3OH)=0.005mol×32g/mol= 0.16g;③ +④×2-①-②,整理可得热化学方程式为CH3OH(l) +O2(g) =CO2(g) +2H2O(l) ΔH=-(c+2d-a-b)kJ/mol
H2↑+Cl2↑+2 OH-;n(NaOH)=0.1mol/L×0.3L=0.03mol,n(e-)=0.03mol,在整个闭合回路中电子转移的数目相等,由于1mol的甲醇反应会失去6mol的电子,所以反应消耗的甲醇的物质的量是0.03mol÷6=0.005mol,甲醇的相对分子质量是32,所以小于消耗甲醇的质量是m(CH3OH)=0.005mol×32g/mol= 0.16g;③ +④×2-①-②,整理可得热化学方程式为CH3OH(l) +O2(g) =CO2(g) +2H2O(l) ΔH=-(c+2d-a-b)kJ/mol
考点:考查化学平衡状态的判断、平衡常数的计算及影响因素、原电池电解池的反应原理及应用、热化学方程式的书写的知识。


科目:高中化学 来源:2014-2015甘肃省天水市高一上学期期末考试化学试卷(解析版) 题型:选择题
化学反应中,有时存在“一种物质过量,另一种物质仍不能完全反应”的特殊情况。下列反应中,属干这种情况的是
①过量锌与18 mol/L的硫酸反应;
②过量氢气与少量氮气在催化剂存在下充分反应;
③浓盐酸与过量的MnO2反应;
④过量铜与浓硫酸反应;
⑤过量稀硝酸与银反应;
⑥过量稀硫酸与大块状石灰石反应。
A.②③④⑥ B.②③⑤ C.①④⑤ D.①②③④⑤⑥
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省岳阳市高三教学质量检测化学试卷(解析版) 题型:选择题
现有四种溶液:①pH=3的CH3COOH溶液,②pH=3的HCl溶液,③pH=11的氨水,④pH=11的NaOH溶液。相同条件下,下列有关上述溶液的叙述中,错误的是
A.①、④等体积混合后,溶液显碱性
B.将②、③溶液混合后,pH=7,消耗溶液的体积:②>③
C.等体积的①、②、④溶液分别与足量铝粉反应,生成H2的量①最大
D.向溶液中加入100 mL水后,溶液的pH:③>④>②>①
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省高三上学期12月联考化学试卷(解析版) 题型:选择题
下列实验设计和结论相符的是
A.在含FeC12杂质的FeCl3溶液中通入足里C12后,充分加热除去过量的C12,即可得到较纯净的FeC13溶液
B.将SO2通入溴水,溴水褪色,说明SO2具有漂白性
C.某无色溶液中加Ba(NO3)2溶液,再加入稀盐酸,沉淀不溶解,则原溶液中一定有SO42-
D.某溶液中加入NaOH溶液并加热,能产生使湿润红色石蕊试纸变蓝的气体,则一定含有NH4+
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省高三上学期12月联考化学试卷(解析版) 题型:选择题
生活中遇到的某些问题,常常涉及到化学知识,下列各项叙述正确的是
A.“加碘盐”、“高钙牛奶”、“富硒营养品”等食用品中的碘、钙、硒是指单质
B.铝合金的大量使用归功于人们能用焦炭等还原剂从氧化铝中获取铝单质
C.医疗上进行胃部造影前,患者服用的“钡餐”是BaCO3等不溶于水的物质
D.“酸可以除锈”、“热的纯碱溶液去油污”,都发生了化学变化
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高三上学期第二次联考理综化学试卷(解析版) 题型:选择题
一定温度下,难溶强电解质的饱和溶液中存在着沉淀溶解平衡,其平衡常数为
物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
Ksp(25℃) | 8.0×10﹣16 | 2.2×10﹣20 | 4.0×10﹣38 |
对于含Fe2(SO4)3、FeSO4和CuSO4各0.5mol的混合溶液1L,根据上表数据判断,说法错误的是
A.向混合溶液中逐滴加入NaOH溶液,最先看到红褐色沉淀
B.向溶液中加入双氧水,并用CuO粉末调节pH,过滤后可获较纯净的CuSO4溶液
C.该溶液中c(SO42﹣):[c(Fe3+)+c(Fe2+)+c(Cu2+)]=5:4
D.将少量FeCl3粉末加入含Cu(OH) 2的悬浊液中,其中c(Cu2+)增大
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省广州市高三1月模拟考试理综化学试卷(解析版) 题型:填空题
(16分)甲烷水蒸气重整制合成气是利用甲烷资源的途径之一,该过程的主要反应是
反应①:CH4(g) + H2O(g)  CO(g) + 3H2(g) ΔH > 0
CO(g) + 3H2(g) ΔH > 0
(1)已知:
CH4(g) + 2O2(g) = CO2(g) + 2H2O(g) ΔH1 = -802 kJ·mol-1
CO(g) + 1/2O2(g) = CO2(g) ΔH2 = -283 kJ·mol-1
H2(g) + 1/2O2(g) = H2O(g) ΔH3 = -242 kJ·mol-1
则反应①的ΔH =_________(用ΔH1、ΔH2和ΔH3表示)。
(2)其他条件相同,反应①在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下反应相同时间后,CH4的转化率随反应温度的变化如图所示。

①在相同条件下,三种催化剂Ⅰ、Ⅱ、Ⅲ的催化效率由高到低的顺序是________。
②a点所代表的状态________(填“是”或“不是”)平衡状态。
③c点CH4的转化率高于b点,原因是________。
(3)反应①在恒容密闭反应器中进行,CH4和H2O的起始物质的量之比为1︰2,10 h后CH4的转化率为80%,并测得c(H2O)=0.132 mol·L-1,计算0~10 h内消耗CH4的平均反应速率_____(写出计算过程,结果保留2位有效数字)。
(4)在答题卡的坐标图中,画出反应①分别在700℃和850℃下进行时,CH4的转化率随时间t变化的示意图(进行必要标注)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省天水市高三一轮复习基础知识检测化学试卷(解析版) 题型:选择题
下列有关溶液中微粒的物质的量浓度关系正确的是
A.1L0.1mol/L (NH4)2Fe(SO4)2溶液:c(SO42-)>c(NH4+)>c(Fe2+)>c(H+)>c(OH-)
B.25℃时,等体积、等浓度的NaX和弱酸HX混合后的溶液中:c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-)
C.25℃时,BaCO3饱和溶液(Ksp=8.1×10-9):c(Ba2+)=c(CO32-)>c(H+)=c(OH-)
D.1.0 mol/L Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+c(H2CO3)
查看答案和解析>>
科目:高中化学 来源:2014-2015吉林省松原市高一上学期期中化学试卷(解析版) 题型:选择题
质量分数为a的某物质的溶液m g与质量分数为b的该物质的溶液n g混合后,蒸发掉p g水,得到的溶液密度为q g/cm3(此过程中无溶质析出),物质的量浓度为c mol·L-1。则溶质的相对分子质量为
A. B.
B.
C. D.
D.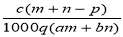
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com