
| A.X=Y=Z | B.X>Y=Z | C.X<Y=Z | D.X=Y<Z |
科目:高中化学 来源:不详 题型:单选题
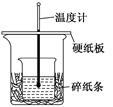
| A.如图条件下实验过程中没有热量损失 |
| B.若改用60 mL 0.50 mol/L盐酸跟50 mL 0.55 mol/L的NaOH溶液进行反应,从理论上说所求反应热相等 |
| C.图中实验装置缺少环形玻璃搅拌棒 |
| D.烧杯间填满碎纸条的作用是固定小烧杯 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.将氢气、酒精设计成燃料电池,是因为燃料电池具有较高的能量利用率,同时氢气、酒精等燃料可再生 |
| B.大力开发丰富的煤炭资源,并将煤进行气化处理,提高煤的综合利用率,可减少对石油的依赖 |
| C.开发和利用太阳能、生物质能、风能等,如在我国西部和沿海地区兴建太阳能、风力发电站等 |
| D.合理开发利用海底可燃冰有助于缓解化石能源紧缺 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.常温下pH=12的烧碱和pH=2的盐酸溶液等体积混合,混合液的pH =7 |
| B.pH相同氨水和烧碱溶液稀释相同倍数时,它们的pH仍相同 |
| C.同浓度盐酸中和pH相同的氨水和烧碱溶液, |
| D.向一定量纯水中通入少量HCl气体后,Kw值增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.40 mL | B.72 mL | C.80 mL | D.128 mL |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.稀硫酸与稀NaOH溶液的中和热为57.3 kJ/mol |
| B.①的反应热为221 kJ/mol |
| C.稀硫酸与稀NaOH溶液反应的中和热为-57.3 kJ/mol |
| D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0︰1︰12︰11 | B.14︰13︰12︰11 | C.14︰13︰2︰3 | D.1︰10︰100︰1000 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.某二元弱酸的酸式盐NaHA溶液中:c(H+)+c(Na+)=c(OH-)+c(HA-)+c(A2-) |
| B.一定量的(NH4)2SO4与NH3·H2O混合所得的酸性溶液中:c(NH4+)<2c(SO42-) |
| C.物质的量浓度均为0.01mol/L的CH3COOH和CH3COONa的溶液等体积混合后溶液中c(CH3COOH)+c(CH3COO-)="0.02" mol/L |
| D.物质的量浓度相等的①NH4HSO4溶液、②NH4HCO3溶液、③NH4Cl溶液中c(NH4-):①>②>③ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 序号 | 氢氧化钡的体积/mL | 盐酸的体积/mL | 溶液的pH |
| ① | 22.00 | 0.00 | 8 |
| ② | 22.00 | 18.00 | 7 |
| ③ | 22.00 | 22.00 | 6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com