
【题目】(1)对下列物质进行系统命名:
 : ;
: ; : 。
: 。
(2) ![]() 的分子式为:__________;
的分子式为:__________;
(3)下列几种烃类物质:

①互为同分异构体的有 和 (写名称)。
②正四面体烷的二氯取代产物有______种;立方烷的二氯取代产物有______种。
(4)某烃类化合物A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振氢谱表明分子中只有一种类型的氢。A的结构简式为 ,名称为_________。A中的碳原子是否都处于同一平面?________(填“是”或“不是”)。
【答案】(1)2,2,4 –三甲基戊烷; 3-甲基苯乙烯 (2) C4H8O (3) ①乙烯基乙炔 正四面体烷
②1;3(4)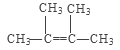 ;2,3-二甲基-2-丁烯 ;是
;2,3-二甲基-2-丁烯 ;是
【解析】
试题分析:(1)该烷烃分子中主链含有5个碳原子,含有3个甲基作支链,其名称是2,2,4 –三甲基戊烷;分子中含有苯环和乙烯基,间位还含有1个甲基,则名称为3-甲基苯乙烯;
(2根据有机物的键线式可知分子式为C4H8O;
(3)①乙烯基乙炔和正四面体烷的分子式相同,均是C4H4,结构不同,互为同分异构体;
②根据有机物结构简式可知正四面体烷的二氯取代产物有1种;立方烷的二氯取代产物有3种,即面对角线、体对角线和面的相邻位置;
(4)A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,则A应为烯烃,设分子式为CnH2n,则有14n=84,n=6,又因为核磁共振氢谱表明分子中只有一种类型的氢,其结构简式应为![]() ,名称为2,3-二甲基-2-丁烯,由于碳碳双键是平面型结构,而4个甲基与不饱和碳原子又直接相连,所以6个碳原子处于同一平面上。
,名称为2,3-二甲基-2-丁烯,由于碳碳双键是平面型结构,而4个甲基与不饱和碳原子又直接相连,所以6个碳原子处于同一平面上。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列有关物质性质的比较,不正确的是
A.金属性:Mg>CaB.稳定性:H2O>H2S
C.酸性:HClO4>H2SO4D.碱性:Mg(OH)2>Al(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是位于短周期的主族元素。已知:①热稳定性:HmD>HmC;②![]() 、
、![]() 具有相同的电子层结构;③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小;④A与B质子数之和是D质子数的3倍。依据上述信息用相应的化学用语回答下列问题:
具有相同的电子层结构;③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小;④A与B质子数之和是D质子数的3倍。依据上述信息用相应的化学用语回答下列问题:
(1)HmDm的电子式___________________。
(2)![]() 、
、![]() 的还原性强弱顺序为:_________,(用离子符号表示)能证明其还原性强弱的离子方程式为________________________________。
的还原性强弱顺序为:_________,(用离子符号表示)能证明其还原性强弱的离子方程式为________________________________。
(3)写出B单质与A元素的最高价氧化物对应水化物的溶液反应的离子方程式:___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】茅台酒中存在少量有凤梨香味的物质X,其结构如右图所示。下列说法正确的是( )

A.X难溶于乙醇
B.酒中的少量丁酸能抑制X的水解
C.分子式为 C4H8O2且官能团与X相同的物质有5种
D.X完全燃烧后生成CO2和H2O的物质的量比为1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨是重要的化工原料,用途广泛。
(1)合成氨工厂常用醋酸二氨合铜(由[Cu(NH3)2]+和CH3COO-构成)溶液吸收对氨合成催化剂(铁粉)有毒害的CO气体。
①醋酸二氨合铜所含的元素中,第一电离能最大的是 。(填元素符号)
②醋酸二氨合铜所含元素的单质,所属的晶体类型有 (填序号)。
a.离子晶体 b.分子晶体 c.原子晶体 d.金属晶体
③第4周期中,基态原子与基态Cu原子未成对电子数目相同的元素有 种(不包括Cu)。
④铜单质为面心立方晶体,其晶胞如图。如果Cu的原子半径为a cm,阿伏加德常数的值为NA,则此种Cu单质的密度表达式为 g/cm3。(相对原子质量Cu:64)


(2)BF3气体与NH3相遇立即生成一种白色晶体:BF3+ NH3=F3B—NH3。写出两种与BF3具有相同空间构型的阴离子 、 。
(3)NH3可用于合成尿素、硫酸铵等氮肥。某化肥厂从生产的硫酸铵中检出一种组成为N4H4(SO4)2的物质。该物质在水溶液中以SO42-和N4H44+两种正四面体构型的离子存在。N4H44+遇碱生成一种形似白磷的N4分子。画出N4H44+的结构(标明其中的配位键) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究发现,NOx和SO2是雾霾的主要成分。
(一)NOx主要来源于汽车尾气。
已知:N2(g)+O2(g)![]() 2NO(g) △H=+180.50 kJ·mol-1
2NO(g) △H=+180.50 kJ·mol-1
2CO(g)+O2(g)![]() 2 CO2(g) △H=-566.00kJ·mol-1
2 CO2(g) △H=-566.00kJ·mol-1
(1)为了减轻大气污染,人们提出在汽车尾气排气管口采用催化剂将NO和CO转化成无污染气体参与大气循环。写出该反应的热化学方程式____________。
(2)T℃时,将等物质的量的NO和CO充入容积为2L的密闭容器中,保持温度和体积不变,反应过程(0-15min)中NO的物质的量随时间变化如图所示。

①T℃时该化学反应的平衡常数K=_________;平衡时若保持温度不变,再向容器中充入CO、N2各0.8 mol,平衡将_______移动。(填“向左”、“向右”或“不”)
②图中a、b分别表示在一定温度下,使用质量相同但表面积不同的催化剂时,达到平衡过程中n(NO)的变化曲线,其中表示催化剂表面积较大的曲线是__________。(填“a”或“b”)
③15min时,若改变外界反应条件,导致n(NO)发生如图所示的变化,则改变的条件可能是____________。
(二)SO2主要来源于煤的燃烧。燃煤烟气的脱硫减排是减少大气中含硫化合物污染的关键。
(3)用纯碱溶液吸收SO2可将其转化为HSO3-。该反应的离子方程式是_____________。
(4)如图电解装置可将雾霾中的NO、SO2分别转化为NH4+和SO42-。
①写出物质A的化学式_____________,阳极的电极反应式是____________Cl。
②该电解反应的化学方程式为________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对复杂的有机物结构可用“键线式”表示。如苯丙烯酸1—丙烯酯: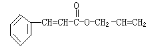 可简化为
可简化为![]() 杀虫剂“阿乐丹”的结构表示为
杀虫剂“阿乐丹”的结构表示为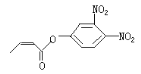 ,若它在稀酸作用下能发生水解反应生成两种有机物,则此两种有机物具有的共同性质是( )
,若它在稀酸作用下能发生水解反应生成两种有机物,则此两种有机物具有的共同性质是( )
A.均能发生银镜反应 B.遇FeCl3溶液均显紫色
C.均能与NaHCO3溶液发生反应 D.均能与浓溴水发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表列出了A~H 8种元素在周期表中的位置:

(1)8 种元素中化学性质最不活泼的是_________(填元素符号);
(2)元素E、F的最高价氧化物对应的水化物反应的离子方程式为______________;
(3)元素D的最低价的氢化物与单质G发生反应的化学方程式为_______________;
(4)写出元素A、C形成的化学式为CA5的电子式____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】周期表中前四周期元素R、W、X、Y、Z的原子序数依次递增。R基态原子中,电子占据的最高能层符号为L,最高能级上只有两个自旋方向相同的电子。工业上通过分离液态空气获得X单质。Y原子的最外层电子数与电子层数之积等于R、W、X三种元素的原子序数之和。Z基态原子的最外能层只有一个电子,其他能层均己充满电子。请回答下列问题:
(1) Z2+基态核外电子排布式为______________。
(2) YX4-的空间构型是______________,与YX4-互为等电子体的一种分子为_____________(填化学式);HYX4酸性比HYX2强,其原因是_____________。
(3)结构简式为RX (W2H3)2的化合物中R原子的杂化轨道类型为_____________;lmo1RX (W2H3) 2分子中含有σ键数目为_____________。
(4)往Z的硫酸盐溶液中通入过量的WH3,可生成[Z(WH3)4]SO4,下列说法正确的是_____________。
A. [Z(WH3)4]SO4中所含的化学键有离子键、极性键和配位键
B.在[Z(WH3)4]2+中Z2+给出孤对电子,NH3提供空轨道
C.在[Z(WH3)4]SO4组成元素中第一电离能最大的是氧元素
(5)某Y与Z形成的化合物的晶胞如图所示(黑点代表Z原子)。

①该晶体的化学式为_____________
②已知Z和Y的电负性分别为1.9和3.0,则Y与L形成的化合物属于_____________(填“离子”、“共价”)化合物。
③已知该晶体的密度为ρg.cm-3,阿伏加德罗常数为NA,则该晶体中Z原子和Y原子之间的最短距离为_____________pm(只写计算式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com