
与100mL 0.5mol·L—1NaCl溶液中的Cl-的物质的量浓度相同的是( )
A.100mL 0.5 mol·L—1MgCl2溶液 B.100mL 0.5mol·L—1 HCl溶液
C.200mL 0.25 mo l·L—1 KCl溶液 D.100 mL 0.5mol·L—1NaClO溶液
mL 0.5mol·L—1NaClO溶液
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:高中化学 来源: 题型:
欲配制100mL 1.0mol•L﹣1Na2SO4溶液,正确的方法是( )
①将14.2g Na2SO4溶于100mL水中
②将32.2gNa2SO4•10H2O溶于少量水 中,再用水稀释至100mL
③将20mL 5.0mol•L﹣1Na2SO4溶液用水稀释至100mL.
|
| A. | ①② | B. | ②③ | C. | ①③ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值,下列说法正确的是
A.1mol CH4含有的电子数为NA
B.标准状况下,2. 24L的CCl4中含有的氯原子数为0.4NA
C.常温常压下,3.0g葡萄糖和冰醋酸的混合物中含有的原子总数为0.4NA
D.标准状况下,2. 24L的乙炔含碳原子数为0.4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
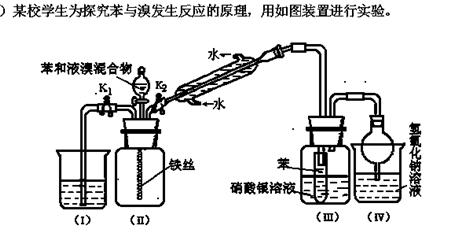
根据相关知识回答下列问题:
(1)实验开始时,关闭K1,开启K2和分液漏斗活塞,滴加苯和液溴的混合液,反应开始。过一会儿,在(III)中可能观察到的现象是 ▲ 。
(2)整套实验装置中能防止倒吸的装置有 ▲ (填装置序号)。
(3)反应结束后要使装置(I)中的水倒吸入装置(II)中。这样操作的目的是 ▲ 。简述这一操作方法 ▲ 。
(4)你认为通过该实验后,有关苯跟溴反应的原理方面能得出的结论是 ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
现有三组溶液:①汽油和氯化钠溶液 ②碘的CCl4溶液 ③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是( )
A.萃取、蒸发、分液 B.分液、蒸馏、萃取
C.分液、萃取、蒸馏 D.蒸馏、萃取、分液
查看答案和解析>>
科目:高中化学 来源: 题型:
某混合气体由N2和CH4组成,测得该混合气体在标准状况下的密度为0.82lg/L,则混合气体中N2和CH4的体积比为( )
A. 1∶1 B. 1∶4 C. 1 ∶ 2 D. 2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
现有25 mL 2 mol·L-1 Na2CO3溶液和75 mL 1 mol·L-1的稀盐酸。①将Na2CO3溶液缓慢滴到稀盐酸中;②将稀盐酸缓慢滴到Na2CO3溶液中,两操作的现象及结果(标准状况下)是( )
A.现象相同,所得气体的体积相等 B.现象相同,所得气体的体积不等
C.现象不同,所得气体的体积相等 D.现象不同,所得气体的体积不等
查看答案和解析>>
科目:高中化学 来源: 题型:
①1molH2O约含 个H2O;
②1molO约含 个e-;
③3× 6.02×1023个电子的物质的量是 mol e-;
④ 1.204×1024个水分子的物质的量为 mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上制备H2的一种重要方法是:
CO(g) + H2O(g)  CO2 (g) + H2(g) △H=Q kJ/mol
CO2 (g) + H2(g) △H=Q kJ/mol
已知
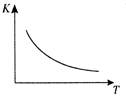
该反应的平衡常数K与温度T的关系右上图所示。若在一固定的密闭容器中,
850℃ 时发生上述反应,测得容器内各物质的浓度 (mol/L)随时间的变化
关系如下表:
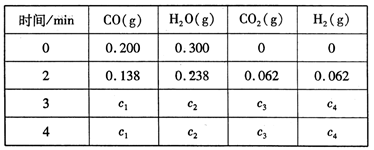
已知:850℃ 时该反应的化学平衡常数K = 1.0 ,请回答下列问题:
(1) Q 0(填“ > ”、“ = ”或“<” )。
若在850℃时向反应容器中充人H2O(g),K 值 (填增大、减小、不变)
(3)上表中 c2为 mol/L , CO(g)的转化率为 (保留三位有效数字)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com