
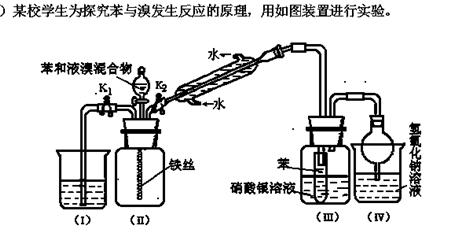
根据相关知识回答下列问题:
(1)实验开始时,关闭K1,开启K2和分液漏斗活塞,滴加苯和液溴的混合液,反应开始。过一会儿,在(III)中可能观察到的现象是 ▲ 。
(2)整套实验装置中能防止倒吸的装置有 ▲ (填装置序号)。
(3)反应结束后要使装置(I)中的水倒吸入装置(II)中。这样操作的目的是 ▲ 。简述这一操作方法 ▲ 。
(4)你认为通过该实验后,有关苯跟溴反应的原理方面能得出的结论是 ▲ 。
科目:高中化学 来源: 题型:
锌是一种应用广泛的金属,目前工业上主要采用“湿法”工艺冶炼锌。某含锌矿的主要成分为ZnS(还含少量FeS等其他成分),以其为原料冶炼锌的工艺流程如下:
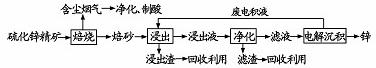
请回答下列问题。
(1)硫化锌精矿的焙烧在氧气气氛的沸腾炉中进行,主要成分发生反应的化学方程式为 。
(2) 焙烧过程中产生的含尘烟气可净化制酸,该酸可用于后续的 操作。工业上制备该酸的三个主要阶段分别为 、 、 。
(3)浸出液“净化”过程中加入的主要物质为 ,其作用是 。
(4)电解沉淀过程中的阴极采用铝板,阳极采用Pb-Ag合金惰性电极,锌在 极沉积,阳极的电极反应方程式为 。
(5)改进的锌冶炼工艺,采用了“氧压酸浸”的全湿法流程,既省略了易导致空气污染的焙烧过程,又可获得一种工业价值的非金属单质。“氧压酸浸”发生主要反应的离子方程式为 。
(6)我国古代曾采用“火法”工艺冶炼锌。明代宋应星著的《天工开物》中有关于“升炼倭铅”的记载:“炉甘石十斤,装载入一泥罐内,……,然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,……,冷淀,毁罐取出,……,即倭铅也。”该炼锌工艺过程主要反应的化学方程式为 。(注:炉甘石的主要成分为碳酸锌,倭铅是指金属锌)
查看答案和解析>>
科目:高中化学 来源: 题型:
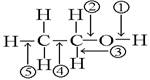
乙醇分子中不同的化学键如图所示,对乙醇在各种反应中应断裂的键说法不正确的是
A.和金属钠作用时,键①断裂
B.和浓硫酸共热至170 ℃时,键②和⑤断裂
C.和乙酸、浓硫酸共热时,键②断裂
D.在银催化下和氧气反应时,键①和③断裂
查看答案和解析>>
科目:高中化学 来源: 题型:
一定质量的乙醇在氧气不足的情况下燃烧,得到CO、CO2和水的总质量为27.6 g,若其中水的质量为10.8 g,则CO的质量是
A. 4.4 g B. 1.4 g C. 2.2 g D. 在2.2 g和4.4 g之间
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质按一定的分类方法属于同一类的是( )
A.酸性氧化物:CO2、SO2、SiO2、Na2O
B.盐: Na2CO3、KHCO3、Cu2(OH)2CO3
C.非电解质:酒精、蔗糖、NH3、次氯酸
D.混合物:液氯、盐酸、胆矾、氯水
查看答案和解析>>
科目:高中化学 来源: 题型:
与100mL 0.5mol·L—1NaCl溶液中的Cl-的物质的量浓度相同的是( )
A.100mL 0.5 mol·L—1MgCl2溶液 B.100mL 0.5mol·L—1 HCl溶液
C.200mL 0.25 mo l·L—1 KCl溶液 D.100 mL 0.5mol·L—1NaClO溶液
mL 0.5mol·L—1NaClO溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
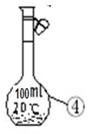
(1)写出下图中序号①~③仪器的名称:

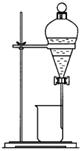
|
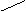
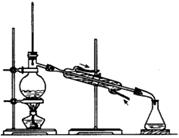
I II III
① ; ② ; ③ 。
 (2)仪器①~④中,使用时必须检查是否漏水的有 。(填仪器序号)
(2)仪器①~④中,使用时必须检查是否漏水的有 。(填仪器序号)
(3)右图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上
的部分内容。现用该浓硫酸配制480 mL 1 mol· L-1的稀硫酸。
可供选用的仪器有:
①胶头滴管②烧瓶③烧杯④ 玻璃棒⑤药匙⑥量筒⑦托盘天平。
请回答下列问题:
a.该硫酸的物质的量浓度为 mol· L-1。
b.配制稀硫酸时,还缺少的仪器有 (写仪器名称)。
c.经计算,配制480mL 1mol· L-1的稀硫酸需要用量筒量取上述浓硫酸的体积为__ mL。
d.对所配制的稀硫酸进行测定,发现其浓度大于1 mol· L-1,配制过程中下列各项操作可能引起该误差的原因有 。
A.定容时,俯视容量瓶刻度线进行定容 。
B.将稀释后的稀硫酸立即转入容量瓶后,紧接着就进行以后的实验操作。
C.转移溶液时,不慎有少量溶液洒到容量瓶外面。
D.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水 。
E.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处。
查看答案和解析>>
科目:高中化学 来源: 题型:
“封管实验”具有简易、方便、节约、绿色等优点,观察下面四个
“封管实验”(夹持装置未画出),判断下列说法正确的是( )
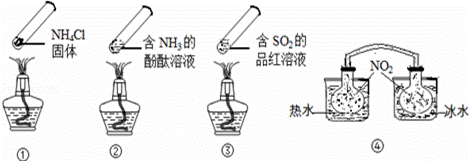
A.加热时,①上部汇集了固体NH4Cl,说明NH4Cl的热稳定性比较好
B.加热时,②、③溶液均变红,冷却后又都变为无色
C.④中,浸泡在热水中的容器内气体颜色变深,浸泡在冰水中的容器内
气体颜色变浅
D.四个“封管实验”中所发生的化学反应都是可逆反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com