
| A. | 铝热剂焊接钢轨主要利用的是光能 | |
| B. | 动物体内葡萄糖被氧化成CO2是热能转变成化学能的过程 | |
| C. | 1g氢气燃烧生成液态水,放出的热量为142.9 kJ,故氢气燃烧热的热化学方程式可以表示为:H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-285.8 kJ/mol | |
| D. | 在温度、压强一定的条件下,自发反应总是向△H-T△S<0的方向进行 |
分析 A.铝具有还原性,能用于冶炼金属;
B.葡萄糖被氧化成CO2是化学能转变成热能;
C.液态水稳定;
D.在温度、压强一定的条件下,△H-T△S<0的反应能够自发进行.
解答 解:A.铝具有还原性,能还原某些金属氧化物,铝热反应不能能还原氧化铁,且放出大量的热,所以利用铝与氧化铁发生的铝热反应来焊接钢轨,故A错误;
B.葡萄糖被氧化成CO2是化学能转变成热能,故B错误;
C.液态水稳定,氢气燃烧热的热化学方程式可以表示为:H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.8 kJ/mol,故C错误;
D.在温度、压强一定的条件下,△H-T△S<0的反应能够自发进行,故D正确;
故选D.
点评 本题考查了能量转化与化学反应的方向问题,明确物质的性质是解本题关键,会运用化学知识解释生活现象,题目难度不大.


科目:高中化学 来源: 题型:解答题
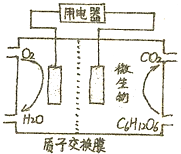 糖类物质为很多生物生命活动提供能量.
糖类物质为很多生物生命活动提供能量.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 裂化汽油 | B. | 直馏汽油 | C. | 甲苯 | D. | 苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢键; 分子间作用力; 非极性键 | |
| B. | 氢键; 氢键; 极性键 | |
| C. | 氢键; 极性键; 分子间作用力 | |
| D. | 分子间作用力; 氢键; 非极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

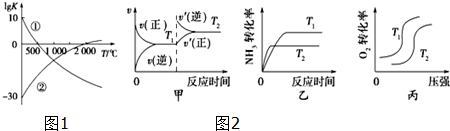
| A. | 图1中醋酸电离平衡常数:a点的比b点的小 | |
| B. | 图1中醋酸溶液的pH:a点的比b点的小 | |
| C. | 图2中c点对应的溶液为Fe(OH)3的不饱和溶液 | |
| D. | 由图2可知,欲除去CuSO4溶液中的Fe3+,可向溶液中加入CuO,调节pH约为4左右 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
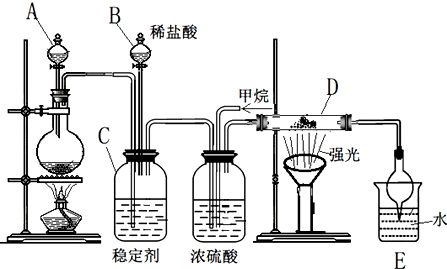
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 卤化氢中,以HF沸点最高,是由于HF分子间存在氢键 | |
| B. | 邻羟基苯甲醛的熔、沸点比对羟基苯甲醛的熔、沸点低 | |
| C. | N2分子中有一个σ键,2个π键 | |
| D. | 在元素周期表中,s区,d区和ds区的元素都是金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com