
��4molSO2��2molO2����2L���ܱ������У���һ�������·�����Ӧ����2s����SO3��Ũ��Ϊ0.6mol��L��1������˵������ȷ����
����O2��ʾ�ķ�Ӧ��ƽ������Ϊ0.6mol��L��1��s��1
����SO2��ʾ�ķ�Ӧ��ƽ������Ϊ0.3mol��L��1��s��1
��2sʱSO2��ת����Ϊ15%
��2sʱO2��Ũ��Ϊ0.7mol��L��1
A�� �٢� B�� �٢� C.���ڢ� D�� �ڢ�

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��1����4molSO2��2molO2����2L���ܱ������У���һ�������·�����Ӧ����10s��ﵽƽ�⣬���SO3��Ũ��Ϊ0.6mol?L-1����ش��������⣺
��1����4molSO2��2molO2����2L���ܱ������У���һ�������·�����Ӧ����10s��ﵽƽ�⣬���SO3��Ũ��Ϊ0.6mol?L-1����ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 5 | 6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
 ���û�ѧ��Ӧԭ���о�Ԫ�ؼ��仯����ķ�Ӧ����������������Ҫ���壮
���û�ѧ��Ӧԭ���о�Ԫ�ؼ��仯����ķ�Ӧ����������������Ҫ���壮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��2012?�Ͳ�һģ�����仯�����ڹ���������ռ����Ҫ�ĵ�λ��
��2012?�Ͳ�һģ�����仯�����ڹ���������ռ����Ҫ�ĵ�λ��| 1 | 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��24�֣�ÿ��3�֣�
(1)��4molSO2��2molO2����2L���ܱ������У���һ�������·�����Ӧ����10s��ﵽƽ�⣬���SO3��Ũ��Ϊ0.6mol��L��1����ش��������⣺
����O2��ʾ�ķ�Ӧ��ƽ������Ϊ_____________________________________
��ƽ��ʱSO2��ת����______________________________________
��ƽ��ʱSO3���������Ϊ___________________________
��10sʱO2��Ũ��Ϊ_____________________________________________
(2)��֪ij���淴ӦmA(g)��nB(g) ![]() qC(g)���ܱ������н��С�
qC(g)���ܱ������н��С�
��ͼ��ʾ��Ӧ�ڲ�ͬʱ��t���¶�T��ѹǿP�뷴Ӧ��B�����
�����Ĺ�ϵ���ߡ�����ͼ�����
�ٻ�ѧ�������Ĺ�ϵ:m��n______q��(�����.������������
�ڸ÷�Ӧ������ӦΪ___________��Ӧ��������ȡ����ȡ���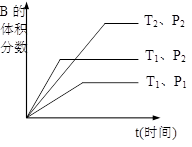
(3)��FeCl3+3KSCNFe(SCN)3+3KCl��ƽ����ϵ�У��ش��������⣺
���������������������
������Һ�м���������KSCN���壬ƽ�� ______________�ƶ���
������Һ�м���������KCl���壬ƽ�� _____________�ƶ���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com