
| 序号 | 甲 | 乙 |
| ① | SO2 | 石灰水 |
| ② | CO2 | 石灰水 |
| ③ | SO2 | Ba(NO3)2 |
| ④ | NO2 | CaCl2 |
| A. | ②③④ | B. | ②③ | C. | ①③④ | D. | ①②③ |
分析 ①二氧化硫与过量的氢氧化钙反应生成亚硫酸钙沉淀;
②二氧化碳与过量的氢氧化钙反应生成碳钙沉淀;
③二氧化硫通入硝酸钡溶液,被硝酸根离子氧化生成硫酸根离子,硫酸根离子与钡离子反应生成硫酸钡;
④二氧化氮与氯化钙溶液中的水反应生成硝酸和一氧化氮,硝酸与氯化钙不反应.
解答 解:①二氧化硫与过量的氢氧化钙反应生成亚硫酸钙沉淀,所以溶液会产生白色的沉淀,故选;
②二氧化碳与过量的氢氧化钙反应生成碳钙沉淀,所以溶液会产生白色的沉淀,故选;
③二氧化硫通入硝酸钡溶液,被硝酸根离子氧化生成硫酸根离子,硫酸根离子与钡离子反应生成硫酸钡,所以溶液会产生白色的沉淀,故选;
④二氧化氮与氯化钙溶液中的水反应生成硝酸和一氧化氮,硝酸与氯化钙不反应,所以溶液不会生成白色沉淀,故不选;
故选:D.
点评 本题考查了反应现象的判断,明确二氧化硫、二氧化碳、二氧化氮的性质是解题关键,注意反应物用量对反应产物的影响,题目难度不大.


 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:多选题
| A. | 剩余固体是铜 | |
| B. | 原固体混合物中铜的质量是9.6g | |
| C. | 反应后溶液中n(Fe3+)=0.10mol | |
| D. | 反应后溶液中n(Fe2+)+n(Cu2+)=0.75mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 配制一定物质的量浓度的溶液时应先用清水润洗容量瓶 | |
| B. | 锥形瓶用作反应容器时一定不能加热 | |
| C. | 蒸馏时温度计水银球可以高于蒸馏瓶支管口 | |
| D. | 振荡分液漏斗时应关闭其玻璃塞和活塞 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
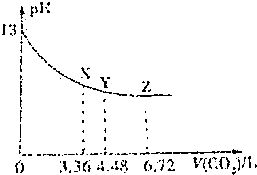
| A. | 该NaOH溶液的浓度为0.1mol/L,体积为6L | |
| B. | X、Y、Z三点对应的溶液中离子的种类不同 | |
| C. | Y点对应的融资中离子浓度关系为:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) | |
| D. | Y点对应的溶液中存在着:c(Na+)=2c(HCO3-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 20s内,H2的浓度改变0.60mol/L,表明该反应达到平衡状态 | |
| B. | 当气体总压强不随时间改变时,表明该反应达到平衡状态 | |
| C. | 使用催化剂会影响达到平衡的时间 | |
| D. | 达到化学平衡状态时,正、逆反应速率都为0且不再发生变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 温度℃ | 25 | 80 | 230 |
| 平衡常数值 | 5×104 | 2 | 1.9×10-5 |
| A. | 上述反应是熵增反应 | |
| B. | 25℃时,反应G(g)?E(s)+4F(g)的平衡常数值是0.5 | |
| C. | 在80℃时,测得某时刻,F、G浓度均为0.5 mol•L-1,则此时v(正)>v(逆) | |
| D. | 恒温恒容下,向容器中再充入少量G(g),达新平衡时,G的体积百分含量将增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com