
【题目】乙烷和乙烯的混合气体200 mL,在催化剂的作用下与氢气发生加成反应,最多消耗氢气100 mL,则原混合气体中乙烷和乙烯的体积比是( )
A. 2∶1B. 3∶1C. 1∶1D. 1∶3
科目:高中化学 来源: 题型:
【题目】下列关于摩尔质量的叙述正确的是( )
A. 氢气的摩尔质量是2 g B. 氢气的摩尔质量就是其相对分子质量
C. 氢的摩尔质量是2 g/mol D. 氢气的摩尔质量是2 g/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葡萄酒中的酒精是葡萄果实中的糖发酵后的产物(C6H12O6 ![]() 2CH3CH2OH+2CO2↑).
2CH3CH2OH+2CO2↑).
Ⅰ、已知:实验室制乙烯原理为CH3CH2OH ![]() CH2=CH2↑+H2O,产生的气体能使Br2 的四氯化碳溶液褪色,甲、乙同学用下列实验验证.(气密性已检验,部分夹持装置略).
CH2=CH2↑+H2O,产生的气体能使Br2 的四氯化碳溶液褪色,甲、乙同学用下列实验验证.(气密性已检验,部分夹持装置略).
实验操作和现象:
操 作 | 现 象 |
点燃酒精灯,加热至170℃ | Ⅰ:A中烧瓶内液体渐渐变黑 |
… | |
实验完毕,清洗烧瓶 | Ⅲ:A中烧瓶内附着少量黑色颗粒状物,有刺激性气味逸出 |
(1)溶液“渐渐变黑”,说明浓硫酸具有性.
(2)分析,甲认为是C2H4 , 乙认为不能排除SO2的作用.
①根据甲的观点,使B中溶液褪色反应的化学方程式是;
②乙根据现象认为实验中产生的SO2和 , 使B中有色物质反应褪色.
(3)为证实各自观点,甲、乙重新实验,设计与现象如下:
甲:在A、B间增加一个装有某种试剂的洗气瓶;现象:Br2的CCl4溶液褪色.
乙:用下列装置按一定顺序与A连接:(尾气处理装置略)
现象:C中溶液由红棕色变为浅红棕色时,E中溶液褪色.
请回答下列问题:
a.甲设计实验中A、B间洗气瓶中盛放的试剂是;乙设计的实验D中盛放的试剂是 , 装置连接顺序为 .
b.能说明确实是SO2使E中溶液褪色的实验是 .
c.乙为进一步验证其观点,取少量C中溶液,加入几滴BaCl2溶液,振荡,产生大量白色沉淀,浅红棕色消失,发生反应的离子方程式是 . 由此可得出的干燥的SO2 不能使Br2 的四氯化碳溶液褪色
Ⅱ、葡萄酒中常用Na2S2O5做抗氧化剂.
(4)0.5molNa2S2O5溶于水配成1L溶液,该溶液的pH=4.5.溶液中部分微粒浓度随溶液酸碱性变化如图所示.写出Na2S2O5溶于水时发生的化学方程式 . 
(5)已知:Ksp[BaSO4]=1×10﹣10 , Ksp[BaSO3]=5×10﹣7 . 把部分被空气氧化的该溶液的pH调为10,向溶液中滴加BaCl2溶液使SO42﹣沉淀完全[c(SO42﹣)≤1×10﹣5molL﹣1],此时溶液中c(SO32﹣)≤molL﹣1 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.某温度下,Ksp(AgCl)=1.8×10﹣10 , Ksp (Ag2CrO4)=1.9×10﹣12 , 故Ag2CrO4更难溶
B.在CaCO3饱和溶液中,加入CaCl2固体,沉淀溶解平衡逆向移动,溶液中Ca2+浓度减小
C.溶度积常数Ksp与温度有关,温度越高,溶度积越大
D.在AgCl饱和溶液中,加入AgCl固体,平衡不移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空
(1)常温下将NaOH溶液和一元弱酸HA溶液混合后.
回答下列问题:
①若将PH=3的HA溶液和PH=11的NaOH溶液等体积混合后,溶液的PH值7(填>、<、=)
②若混合后溶液PH值等于7,则混合后溶液中各离子浓度大小次序为 .
(2)已知常温下Ksp[Al(OH)3]=3×10﹣34;Ksp[Fe(OH)3]=4×10﹣38在25℃向浓度均为0.1mol/L的AlCl3和FeCl3混合溶液中逐滴加入氨水,
请写出最先生成沉淀的离子方程式 . 当溶液PH=10时,C(Al3+)=mol/L
(3)1909年化学家哈伯在实验室首次合成了氨.氨的应用较多,据此回答下列问题:合成氨反应的化学方程式为N2(g)+3H2(g)2NH3(g);
①写出该反应的平衡常数表达式:K= .
②在一定条件下的2L密闭容器中进行实验,并测得下列数据
物质 | N2 | H2 | NH3 |
起始(mol) | 2 | 7 | 0 |
10s(mol) | 1.6 | ||
平衡(mol) | 2 |
平衡时,N2的转化率为 .
③在一定温度,一定体积的密闭容器中进行合成氨的实验,下列不可以判断反应达到平衡状态的为 .
A、密度保持不变
B、平均分子量保持不变
C、气体的总物质的量保持不变
D、单位时间内每消耗1molN2的同时生成2mol氨气
④汽车尾气中含有较多的NO2和NO若任意排放可形成光化学烟雾,利用NH3可将其除去,同时得到不会污染空气的物质,试写出NH3与NO2反应的化学化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2S2O3在化学定量分析中常用作基准物质,遇酸易分解;实验室制备原理为2Na2S+Na2CO3+4SO2 ![]() 3Na2S2O3+CO2 . 实验装置如下:
3Na2S2O3+CO2 . 实验装置如下: 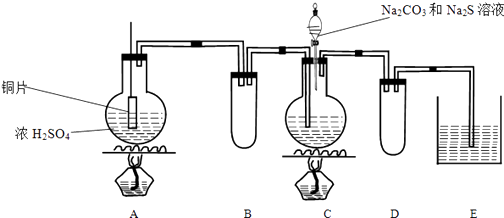
(1)A中发生反应的化学方程式是: .
(2)E中所盛试剂作用是;若要停止A中的化学反应,还可以采取的操作是 .
(3)B和D装置作用:
(4)甲同学在加热A后,发现液面下的铜丝变黑.该同学对黑色生成物提出如下假设:
①可能是CuO;②可能是Cu2O;③可能是CuS
乙同学认为假设②一定不成立,依据是 .
该同学设计实验进一步验证黑色物质的组成:
基于上述假设分析,黑色物质的组成为(填化学式) .
(5)C中通入SO2不能过量原因是 .
(6)实验室用硫代硫酸钠溶液吸收残余氯气生成SO42﹣ , 其反应的离子方程式是:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pH=2的A,B两种酸溶液各1mL,分别加水稀释到1000mL,其中pH与溶液体积V的关系如图所示.下列说法正确的是( ) 
A.A,B两酸溶液的物质的量浓度一定相等
B.稀释后,A酸溶液的酸性比B酸溶液强
C.a=5时,A是强酸,B是弱酸
D.若a小于5,则A,B都是弱酸,且A的酸性弱于B
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2010年,中国首次应用六炔基苯在铜片表面合成了石墨炔薄膜(其合成示意图如图所示),其特殊的电子结构将有望广泛应用于电子材料领域.下列说法不正确的是( ) 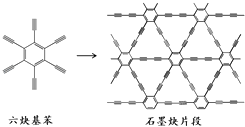
A.六炔基苯的化学式为C18H6
B.六炔基苯和石墨炔都具有平面型结构
C.六炔基苯和石墨炔都可发生加成反应
D.六炔基苯合成石墨炔属于加聚反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com