
 1、实验室要配制物质的量浓度为0.1mol/L的NaOH溶液480mL
1、实验室要配制物质的量浓度为0.1mol/L的NaOH溶液480mL| 配制时应称量 NaOH的质量/g | 已给仪器 | 配制时除已给仪器外 还需要的其他仪器 |
| ______ | 烧杯、药匙、 托盘天平 | ______ |
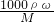 可知,还缺少该溶液的密度,故答案为:该溶液的密度;
可知,还缺少该溶液的密度,故答案为:该溶液的密度;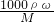 可知,还缺少该溶液的密度;
可知,还缺少该溶液的密度; 分析操作对所配溶液浓度的影响;
分析操作对所配溶液浓度的影响; 理解溶液的配制与误差分析.
理解溶液的配制与误差分析. 

科目:高中化学 来源: 题型:
 1、实验室要配制物质的量浓度为0.1mol/L的NaOH溶液480mL
1、实验室要配制物质的量浓度为0.1mol/L的NaOH溶液480mL| 配制时应称量 NaOH的质量/g |
已给仪器 | 配制时除已给仪器外 还需要的其他仪器 |
2.0 2.0 |
烧杯、药匙、 托盘天平 |
500mL容量瓶、玻璃棒、胶头滴管 500mL容量瓶、玻璃棒、胶头滴管 |
查看答案和解析>>
科目:高中化学 来源:2011-2012学年河南省高三上学期10月份月考化学试卷 题型:实验题
(12分) 某同学在实验室欲配制物质的量浓度均为1.0 mol/L的NaOH溶液和稀H2SO4各450mL。提供的试剂是:NaOH固体和98%的浓H2SO4(密度为1.84 g/cm3)及蒸馏水。
(1)配制两种溶液时都需要的玻璃仪器是____________________________________ 。
(2)应用托盘天平称量NaOH ___________g,应用量筒量取浓H2SO4________mL。
(3)配制时,先要检查容量瓶是否漏水,其方法是
。
(4)浓硫酸溶于水的正确操作方法是_____ ___________。
(5)在配制上述溶液实验中,下列操作引起结果偏低的有_________________
A.该学生在量取浓硫酸时,俯视刻度线
B.称量固体NaOH时,将砝码和物品的位置颠倒(没有使用游码)
C.溶解H2SO4操作时没有冷却至室温就立即完成后面的配制操作。
D.在烧杯中溶解搅拌时,溅出少量溶液
E.没有用蒸馏水洗烧杯2—3次,并将洗液移入容量瓶中
F.将量筒洗涤2—3次,并全部转移至容量瓶中
G.容量瓶中原来存有少量蒸馏水
H.胶头滴管加水定容时俯视刻度
查看答案和解析>>
科目:高中化学 来源: 题型:
(12分) 某同学在实验室欲配制物质的量浓度均为1.0 mol/L的NaOH溶液和稀H2SO4各450mL。提供的试剂是:NaOH固体和98%的浓H2SO4(密度为1.84 g/cm3)及蒸馏水。
(1)配制两种溶液时都需要的玻璃仪器是____________________________________ 。
(2)应用托盘天平称量NaOH ___________g,应用量筒量取浓H2SO4________mL。
(3)配制时,先要检查容量瓶是否漏水,其方法是
。
(4)浓硫酸溶于水的正确操作方法是_____ ___________。
(5)在配制上述溶液实验中,下列操作引起结果偏低的有_________________
A.该学生在量取浓硫酸时,俯视刻度线
B.称量固体NaOH时,将砝码和物品的位置颠倒(没有使用游码)
C.溶解H2SO4操作时没有冷却至室温就立即完成后面的配制操作。
D.在烧杯中溶解搅拌时,溅出少量溶液
E.没有用蒸馏水洗烧杯2—3次,并将洗液移入容量瓶中
F.将量筒洗涤2—3次,并全部转移至容量瓶中
G.容量瓶中原来存有少量蒸馏水
H.胶头滴管加水定容时俯视刻度
查看答案和解析>>
科目:高中化学 来源:2012届河南省郑州市智林学校高三上学期10月份月考化学试卷 题型:实验题
(12分) 某同学在实验室欲配制物质的量浓度均为1.0 mol/L的NaOH溶液和稀H2SO4各450mL。提供的试剂是:NaOH固体和98%的浓H2SO4(密度为1.84 g/cm3)及蒸馏水。
(1)配制两种溶液时都需要的玻璃仪器是____________________________________ 。
(2)应用托盘天平称量NaOH ___________g,应用量筒量取浓H2SO4________mL。
(3)配制时,先要检查容量瓶是否漏水,其方法是
 。
。
(4)浓硫酸溶于水的正确操作方法是_____ ______ _____。
_____。
(5)在配制上述溶液实验中,下列操作引起结果偏低的有_________________
| A.该学生在量取浓硫酸时,俯视刻度线 |
| B.称量固体NaOH时,将砝码和物品的位置颠倒(没有使用游码) |
C.溶解H2SO4操作时没有冷却至室温就立即完成后面的配制操 作。 作。 |
D.在烧杯中溶解 搅拌时,溅出少量溶液 搅拌时,溅出少量溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com