
【题目】在配制Fe2(SO4)3溶液时,为了防止水解,常常往溶液中加入少量的
A.NaOHB.H2SO4C.KClD.CH3COOH
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】欲配制下列四种无色透明的酸性溶液,其中能配制成功的是
A.NH4+、NO3-、Al3+、Cl-B.Na+、Fe3+、OH-、NO3-
C.MnO4-、K+、SO42-、Na+D.Ca2+、Mg2+、HCO3-、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Mg原子最外层电子数为_____,反应中容易________个电子而显示_____价; F原子最外层电子数为_____,反应中容易__________个电子而显示_____价。在上述过程中,F原子和 Mg原子通过_____________都形成了8电子稳定结构。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.1000mol/L NaOH溶液滴定20.00mL 0.1000mol/L HCl溶液,滴定曲线如图所示,下列说法不正确的是
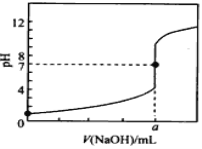
A. a=20.00
B. 滴定过程中,可能存在:c(Cl-)>c(H+)>c(Na+)>c(OH-)
C. 若将盐酸换成相同浓度的醋酸,则滴定到pH=7时,a<20.00
D. 若用酚酞作指示剂,当滴定到溶液明显由无色变为浅红色时立即停止滴定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】700℃时,H2(g)+CO2(g)![]() H2O(g)+CO(g)。该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2和CO2,起始浓度如下表所示。其中甲经2min达平衡时,v(H2O)为0.025 mol/(L·min),下列判断不正确的是()
H2O(g)+CO(g)。该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2和CO2,起始浓度如下表所示。其中甲经2min达平衡时,v(H2O)为0.025 mol/(L·min),下列判断不正确的是()
起始浓度 | 甲 | 乙 | 丙 |
C(H2)/mol/L | 0.1 | 0.2 | 0.2 |
C(CO2)/mol/L | 0.1 | 0.1 | 0.2 |
A. 平衡时,乙中CO2的转化率大于50%
B. 当反应平衡时,丙中c(CO2)是甲中的2倍
C. 温度升至800℃,上述反应平衡常数为25/16,则正反应为吸热反应
D. 其他条件不变,若起始时向容器乙中充入0.10mol/L H2和0.20 mol/L CO2,到达平衡时c (CO)与乙不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如下:

(1)反应Ⅰ:2H2SO4(l)=2SO2(g)+O2(g)+2H2O(g) ΔH=+550 kJ·mol-1
它由两步反应组成:i. H2SO4(l)=SO3(g)+H2O(g) ΔH=+177 kJ·mol-1 ii. SO3(g)分解。
L(L1、L2)、X可分别代表压强和温度。下图表示L一定时,ii中SO3(g)的平衡转化率随X的变化关系。

① X代表的物理量是_____________________。
② 判断L1、L2的大小关系是______________。
(2)反应Ⅱ:I-可以作为催化剂,可能的催化过程如下。
i. SO2+4I-+4H+=S↓+2I2+2H2O; ii. I2+2H2O+ SO2= SO42-+4H++2I-;
探究i、ii反应速率与SO2歧化反应速率的关系,实验如下:分别将18 mL SO2饱和溶液加入到2 mL下列试剂中,密闭放置观察现象。(已知:I2易溶解在KI溶液中)
序号 | A | B | C | D |
试剂组成 | 0.4 mol/L KI | a mol/LKI 0.2 mol/LH2SO4 | 0.2 mol/L H2SO4 | 0.2 mol/L KI 0.0002 mol I2 |
实验现象 | 溶液变黄,一段时间后出现浑浊 | 溶液变黄,出现浑浊较A快 | 无明显现象 | 溶液由棕褐色很快褪色,变成黄色,出现浑浊较A快 |
① B是A的对比实验,则a=__________。
② 比较A、B、C,可得出的结论是_______________________________。
③ 实验表明,SO2的歧化反应速率D>A,结合i、ii反应速率解释原因:___________。
(3)在钠碱循环法中,Na2SO3溶液作为吸收液吸收SO2的过程中,pH随n(SO32-):n(HSO3-)变化关系如下表:
n(SO32-):n(HSO3-) | 91:9 | 1:1 | 1:91 |
pH | 8.2 | 7.2 | 6.2 |
当吸收液的pH降至约为6时,需送至电解槽再生。再生示意图如下:

① 上表判断NaHSO3溶液显__________性,用化学平衡原理解释:_____________。
② HSO3-在阳极放电的电极反应式是______,当阴极室中溶液pH升至8以上时,吸收液再生并循环利用。简述再生原理________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)氯碱工业中电解饱和食盐水流程及原理示意图如下图所示。
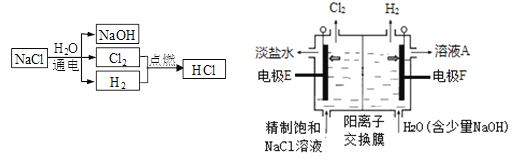
(1)生成H2的电极反应式是_________________________________________。
(2)Na+向________(填“E”或“F”)方向移动,溶液A的溶质是______________。
(3)电解饱和食盐水总反应的离子方程式是_____________________________。
(4)常温下,将氯碱工业的附属产品盐酸与氨水等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表。
实验编号 | 氨水浓度/mol·L-1 | 盐酸浓度/mol·L-1 | 混合溶液pH |
① | 0.1 | 0.1 | pH=5 |
② | c | 0.2 | pH=7 |
③ | 0.2 | 0.1 | pH>7 |
ⅰ. 实验①中所得混合溶液,由水电离出的c(H+)=______ mol·L-1。
ⅱ. 实验②中,c______0.2(填“>”“<”或“=”)。
ⅲ. 实验③中所得混合溶液,各离子浓度由大到小的顺序是__________________。
ⅳ. 实验①、③所用氨水中的![]() :①___________③(填“>”“<”或“=”)。
:①___________③(填“>”“<”或“=”)。
(5)氯在饮用水处理中常用作杀菌剂,且HClO的杀菌能力比ClO-强。25℃时氯气-氯水体系中的Cl2(aq)、HClO和ClO-分别在三者中所占分数(α)随pH变化的关系如下图所示。

下列表述正确的是_______。
A. 氯处理饮用水时,在夏季的杀菌效果比在冬季好
B. 在氯处理水体系中,c(HClO)+c(ClO-)=c(H+)-c(OH-)
C. 用氯处理饮用水时,pH=7.5时杀菌效果比pH=6.5时效果差
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲苯(![]() )是一种重要的化工原料,能用于生产苯甲醛(
)是一种重要的化工原料,能用于生产苯甲醛(![]() )、苯甲酸(
)、苯甲酸(![]() )等产品。下表列出了有关物质的部分物理性质,请回答:
)等产品。下表列出了有关物质的部分物理性质,请回答:
名称 | 性状 | 熔点(℃) | 沸点(℃) | 相对密度 (ρ水=1g/cm3) | 溶解性 | |
水 | 乙醇 | |||||
甲苯 | 无色液体易燃易挥发 | -95 | 110.6 | 0.8660 | 不溶 | 互溶 |
苯甲醛 | 无色液体 | -26 | 179 | 1.0440 | 微溶 | 互溶 |
苯甲酸 | 白色片状或针状晶体 | 122.1 | 249 | 1.2659 | 微溶 | 易溶 |
注:甲苯、苯甲醛、苯甲酸三者互溶。
实验室可用如图装置模拟制备苯甲醛。实验时先在三颈瓶中加入0.5g固态难溶性催化剂,再加入15mL冰醋酸(作为溶剂)和2mL甲苯,搅拌升温至70℃,同时缓慢加入12mL过氧化氢,在此温度下搅拌反应3小时。

(1)装置a的名称是__________________,主要作用是____________________。
(2)三颈瓶中发生反应的化学方程式为_______________________________________,此反应的原子利用率理论上可达___________。(原子利用率=(期望产物的总质量/全部反应物的总质量)×100%)
(3)经测定,反应温度升高时,甲苯的转化率逐渐增大,但温度过高时,苯甲醛的产量却有所减少,可能的原因是________________________________________________。
(4)反应完毕后,反应混合液经过自然冷却至室温时,还应经过 ________、________(填操作名称)等操作,才能得到苯甲醛粗产品。
(5)实验中加入过量过氧化氢且反应时间较长,会使苯甲醛产品中产生较多的苯甲酸。若想从混有苯甲酸的苯甲醛中分离出苯甲酸,正确的操作步骤是_______(按步骤顺序填字母)。
a.对混合液进行分液 b.过滤、洗涤、干燥
c.层中加入盐酸调节pH=2 d.加入适量碳酸氢钠溶液混合震荡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,硫氢化钾溶液里存在下列平衡:
a.HS-+H2O![]() OH-+H2S b.HS-
OH-+H2S b.HS-![]() H++S2-
H++S2-
(1)平衡a是_________平衡;平衡b是_________平衡。(填“电离”或“水解”)
(2)向KHS溶液中加入氢氧化钠固体时,c(S2-)将_________(填“增大”“城小”或“不变”。下同);向KHS溶液中通入HCl时,c(HS-)将_________。
(3)向KHS溶液中加入硫酸铜溶液时,有黑色沉淀(CuS)产生,则平衡a_________(填“正向”“逆向”或“不”,下同)移动,平衡b_________移动;溶液的pH_________(填“增大”“減小”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com