
分析 (1)氯气具有强氧化性,氧化变价金属市场高价化合物,氯气和铁反应生成氯化铁;
(2)浓硝酸具有强氧化性,可在常温下与铝、铁发生钝化反应;
(3)可用于焊接钢轨需要反应放热生成的金属呈熔融状态;
(4)在空气中迅速变为灰绿色,最后变为红褐色,是Fe(OH)2遇到氧气会被氧气氧化成Fe(OH)3;
(5)三价铁离子遇到KSCN溶液会生成血红色溶液,是铁离子的检验方法.
解答 解:(1)将烧得红热的铁丝伸到盛有氯气的集气瓶中,可观察到有棕黄色的烟生成,产物为氯化铁固体,反应的化学方程式为:2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2FeCl3,
故答案为:2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2FeCl3;
(2)金属钝化的实质是金属被浓硫酸、浓硝酸氧化,表面生成一层致密的氧化膜,这种氧化膜不溶于浓硫酸、浓硝酸.,铁、铝在常温下与浓硝酸发生钝化,是因为浓硝酸具有强氧化性,在金属的表面生成一层致密的氧化物膜,阻碍反应的继续进行,
故答案为:氧化;
(3)①3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$ 2Fe+3CO2,反应在高温下进行生成铁,但在野外条件下难于实现反应,
②2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$ 2Fe+Al2O3 ,氯和氧化铁反应是放热反应,放出的热量使生成的铁呈熔融状态,可以焊接钢轨,
③3Fe+4H2O(g)$\frac{\underline{\;\;△\;\;}}{\;}$ Fe3O4+4H2 ,反应是吸热反应,不能焊接钢轨,
故答案为:②;
(4)在空气中迅速变为灰绿色,最后变为红褐色,是Fe(OH)2遇到空气中的氧气,会被氧气氧化成Fe(OH)3,反应方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:空气中氧气;
(5)在两支试管里分别加入5mL FeCl2溶液和5mL FeCl3溶液,各滴入几滴KSCN溶液,可观察到溶液变为红色现象的是氯化铁溶液,Fe3++3SCN-=Fe(SCN)3,
故答案为:氯化铁.
点评 本题考查了元素化合物性质的分析应用,主要是铁及其化合物、浓硝酸、金属冶炼、铝热反应、离子检验等知识的理解应用,掌握基础是解题关键,题目难度不大.


科目:高中化学 来源:2017届江苏省高三上第一次测试化学试卷(解析版) 题型:选择题
有Fe2++H++NO3-→Fe3++NH4++H2O这样一个变化过程,下列叙述不正确的是
A.氧化剂和还原剂的物质的量之比为1:8
B.该过程说明Fe(NO3)2溶液不宜加酸酸化
C.每1 mol NO3-发生氧化反应,转移8 mol 电子
D.若把该反应设计为原电池,则负极反应为Fe2+-e- = Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
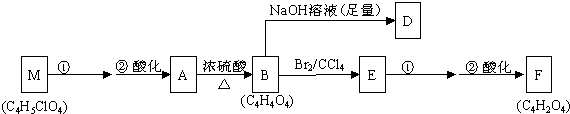
 +n HOCH2CH2OH$\stackrel{一定条件}{→}$
+n HOCH2CH2OH$\stackrel{一定条件}{→}$ +(2n-1)H2O.
+(2n-1)H2O. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解法:MgCl2$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑ | |
| B. | 热还原法:Fe2O3+3CO$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+3CO2 | |
| C. | 热分解法:2Al2O3═4Al+3O2↑ | |
| D. | 物理方法:利用密度大的性质水洗矿物提取金 |
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三上第一次测试化学试卷(解析版) 题型:选择题
下列有关化学用语表示正确的是
A.CaH2的电子式:[H:]‑Ca2+[:H]-
B.Cl-的结构示意图:
C.质子数为92、中子数为146的U原子: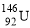
D.2,4,6-三硝基苯甲酸结构简式:
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
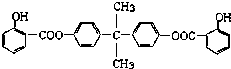
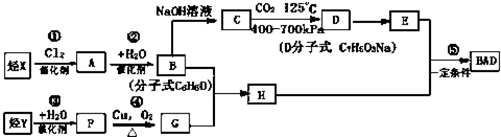
 .
. .F+E
.F+E .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
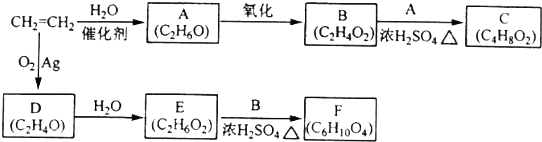
 ;
;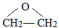 ;
;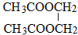 ;
;查看答案和解析>>
科目:高中化学 来源:2017届江苏省如皋市高三上学期质量调研一化学试卷(解析版) 题型:填空题
将不可再生的天然气、石油、煤等化石燃料转化利用、变废为宝已成为当务之急。
(1)根据键能数据估算CH4+4F2=CF4+4HF的反应热ΔH= 。
化学键 | C—H | C—F | H—F | F—F |
键能/(kJ·mol-1) | 414 | 489 | 565 | 155 |
(2)甲醇、二甲醚(CH3OCH3)被称为21世纪的新型燃料,均可利用CO和H2反应合成。
①某燃料电池以二甲醚为原料,熔融碳酸盐为电解质,其负极反应如下:
CH3OCH3+6CO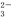 -12e-=8CO2+3H2O。写出该燃料电池的正极反应式: 。
-12e-=8CO2+3H2O。写出该燃料电池的正极反应式: 。
②废水中含甲醇对水质会造成污染,Co3+可将甲醇氧化为CO2。某同学以Pt作电极电解酸性含甲醇废水与CoSO4混合液模拟工业除污原理,其阳极反应式为 。
(3)某企业采用如图所示原理处理化石燃料开采、加工过程产生的H2S废气。
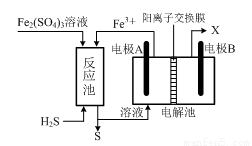
①电解池中电极A、B均为惰性电极,其中A为电解池的 极;电极B所得到的物质X的分子式为 。
②反应池中发生的离子反应方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com