
| A、C4H10 |
| B、C3H8 |
| C、C3H8O |
| D、C2H4O2 |
| 7.2g |
| 18g/mol |
| 13.2g |
| 44g/mol |
| 1.6g |
| 16g/mol |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
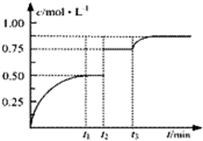 一定温度下,将1molA和1molB气体充入2L密闭容器,发生反应:A(g)+B(g)?xC(g)+D(s),t1时达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示.下列说法正确是( )
一定温度下,将1molA和1molB气体充入2L密闭容器,发生反应:A(g)+B(g)?xC(g)+D(s),t1时达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示.下列说法正确是( )| A、t1~t3间该反应的平衡常数均为4 |
| B、反应方程式中的x=1 |
| C、t2时刻改变的条件是使用催化剂 |
| D、t3时刻改变的条件是移去少量物质D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 实验目的或结论 |
| A | 向某溶液中加入盐酸,产生CO2气体 | 说明原溶液中一定为Na2CO3 |
| B | 向某溶液中滴入氢氧化钠溶液,产生蓝色沉淀 | 说明原溶液中一定含有Cu2+ |
| C | 向某溶液中滴入氯化钡溶液,产生白色沉淀 | 说明原溶液中一定含有Ag+ |
| D | 向某溶液中先滴入盐酸,再滴入氯化钡溶液,产生白色沉淀 | 说明原溶液中一定含有SO42- |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| O | 2- 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、检验SO42-:加入BaCl2溶液出现白色沉淀,再加足量稀HCl沉淀不溶解 |
| B、检验Cl-:加入AgNO3溶液出现白色沉淀 |
| C、检验Na+:将干净的铂丝蘸取少量溶液灼烧,观察火焰呈黄色 |
| D、检验NH4+:滴入NaOH溶液后,加热,用湿润蓝色石蕊试纸检验发现变红 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②⑤⑥③④ |
| B、③⑤④⑥①② |
| C、④③⑥⑤①② |
| D、④③⑤⑥②① |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①⑤③⑥④② |
| B、①⑤③④⑥② |
| C、①③④⑥⑤② |
| D、①③⑤⑥④② |
查看答案和解析>>
科目:高中化学 来源: 题型:
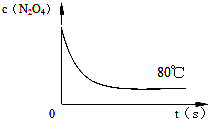
时间 (s) c(mol?L-1) | 0 | 20 | 40 | 60 | 80 | 100 |
| c(N2O4) | 0.20 | a | 0.10 | C | d | e |
| c(NO2) | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaCl溶液蒸发结晶时,蒸发皿中有大量晶体析出即停止加热 |
| B、用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 |
| C、在50mL量筒中配制0.10mol/L的碳酸钠溶液 |
| D、将Mg(OH)2浊液直接倒入已装好滤纸的漏斗中过滤,洗涤并收集沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com