
【题目】共价键的断裂有均裂和异裂两种方式,即均裂:AB―→A![]() ,异裂:AB―→A++[B]-。下列化学反应中发生共价键均裂的是( )
,异裂:AB―→A++[B]-。下列化学反应中发生共价键均裂的是( )
A. 2K+2H2O===2KOH+H2↑
B. 2Na+2C2H5OH―→2C2H5ONa+H2↑
C. Na2CO3+H2O![]() NaHCO3+NaOH
NaHCO3+NaOH
D. CH3COOH+C2H5OH![]() H2O+CH3COOC2H5
H2O+CH3COOC2H5
【答案】D
【解析】A、B、C三项都是异裂,只有D才是均裂,判断的关键是看有没有形成阴阳离子,如果有则是异裂。
根据题中信息可知:均裂后形成共价化合物,异裂后产生离子化合物,A.反应2K+2H2O=2KOH+H2↑中,水中共价键形成了离子键,属于共价键异裂,选项A错误;B.反应2Na+2C2H5OH―→2C2H5ONa+H2↑中,乙醇羟基形成了离子键,属于共价键异裂,选项B错误;C.反应Na2CO3+H2O![]() NaHCO3+NaOH中,水中共价键断裂生成离子化合物氢氧化钠,属于共价键异裂,选项C错误;D.反应CH3COOH+C2H5OH
NaHCO3+NaOH中,水中共价键断裂生成离子化合物氢氧化钠,属于共价键异裂,选项C错误;D.反应CH3COOH+C2H5OH![]() H2O+CH3COOC2H5中,共价键断裂生成了共价化合物,属于共价键均裂,选项D正确;答案选D。
H2O+CH3COOC2H5中,共价键断裂生成了共价化合物,属于共价键均裂,选项D正确;答案选D。


科目:高中化学 来源: 题型:
【题目】有机物X(分子式为C4H6O5)广泛存在于许多水果中,尤以苹果、葡萄、西瓜、山楂内为多。经测定该有机物具有下列性质(见下表)。请根据题目要求填空:
X的性质 | |
① | X与足量的金属钠反应产生氢气 |
② | X与醇或羧酸在浓硫酸加热条件下均能生成有香味的产物 |
③ | 在一定条件下X的分子内脱水产物(不是环状化合物)可与溴水发生加成反应 |
④ | 33.5gX与100mL的5mol/LNaOH溶液恰好完全中和 |
(1)X的可能结构简式I:________,Ⅱ:__________,Ⅲ:__________。
(2)在一定条件下有机物X可发生化学反应的类型有(填序号)__________。
A.水解反应 B.取代反应 C.加成反应 D.消去反应 E.加聚反应 F.中和反应
(3)下列物质与X互为同系物的是(填序号)_______,与X互为同分异构体的是(填序号)_______。
(a)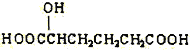 (b)
(b)![]()
(c)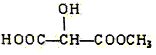 (d)H3COOC-COOCH3
(d)H3COOC-COOCH3
(e)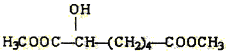 (f)
(f)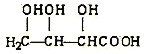
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组通过查阅资料得知,CO2与Na2O2的反应需要在一定量水蒸气存在的条件下才能进行,于是他们设计了如图所示的装置对此问题进行探究,同时验证Na2O2与CO2反应的气体产物。

(1)写出装置A中有关反应的离子方程式:_________________,装置B中的试剂是____,装置E的作用是_____________。
(2)U形管C中的试剂是____。若要求根据装置D中的现象来确定CO2与Na2O2之间的反应是否需要在潮湿的条件下才能进行,对两个止水夹的操作方式为先打开K1,关闭K2,D中无明显现象;当打开K2,关闭K1,D中的现象为 ______________,则说明反应需要在潮湿条件下进行。
(3)检验气体产物的方法:用玻璃片在水里盖住集气瓶口,将集气瓶从水中取出,正放在实验台上,_______________。
(4)有人认为,经过较长时间反应后,装置D中生成的物质只有Na2CO3而没有NaOH。请设计一个方案证明此结论是正确的:______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列过程有热量放出的是( )
A. 化学反应中形成氢气中的HH键
B. C(s)与H2O(g)反应
C. H2O(l)转化为H2O(s)
D. H2O2分解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y的核电荷数分别是a和b,它们的离子Xn+和Ym-的核外电子排布相同,则下列关系式中正确的是( )
A. a=b+m+n B. a=b-m+n
C. a=b+m-n D. a=b-m-n
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛的化合物如TiO2、Ti(NO3)4、TiCl4、Ti(BH4)2等均有着广泛用途。
(1)写出Ti的基态原子的外围电子排布式_____。
(2)TiCl4熔点是﹣25℃,沸点136.4℃,可溶于苯或CCl4,该晶体属于_____晶体;BH4﹣中B原子的杂化类型为_____。
(3)在 TiO2催化作用下,可将CN﹣氧化成CNO﹣,进而得到N2。与CNO﹣互为等电子体的分子化学式为(只写一种)________。
(4)Ti3+可以形成两种不同的配合物:[Ti(H2O)6]Cl3(紫色),[TiCl(H2O)5]Cl2H2O(绿色)。绿色晶体中配体是_______。

(5)TiO2难溶于水和稀酸,但能溶于浓硫酸,析出含有钛酰离子的晶体,钛酰离子常成为链状聚合形式的阳离子,其结构形式如图1,化学式为______。
(6)金属钛内部原子的堆积方式是面心立方堆积方式,如图2。若该晶胞的密度为ρgcm﹣3,阿伏加德罗常数为NA,则该晶胞的边长为___cm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对于某些离子的检验及结论中一定正确的
A. 加入稀盐酸产生无色的气体,将气体通入澄清石灰水中,溶液变浑浊,一定有![]()
B. 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有![]()
C. 加入氢氧化钠溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝,一定有![]()
D. 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 钢铁表面水膜酸性很弱或呈中性,发生吸氧腐蚀

B. 钢铁表面水膜酸性较强,发生析氢腐蚀

C. 钢闸门作为阴极而受到保护

D. 将锌板换成铜板对钢闸门保护效果更好

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com