
【题目】下列说法正确的是( )
A. 做衣服的棉、麻、蚕丝的主要成分都是纤维素
B. 油脂在碱性条件下的水解为皂化反应
C. 石油的分馏和煤的干馏都是物理变化
D. 饱和Na2SO4、CuSO4溶液均可用于蛋白质的盐析
科目:高中化学 来源: 题型:
【题目】用Na2CO3·10H2O晶体,配制0.2 mol·L-1的Na2CO3溶液480 mL。
(1)应称取Na2CO3·10H2O晶体的质量:____________。定容时,向容量瓶中加水,至1~2cm时,改用_________加水至刻度,加盖摇匀;
(2)根据下列操作对所配溶液的浓度产生的影响,完成下列要求:
①Na2CO3·10H2O晶体失去了部分结晶水 ②用“左码右物”的称量方法称量晶体(使用游码) ③碳酸钠晶体不纯,其中混有氯化钠 ④称量碳酸钠晶体时所用砝码生锈 ⑤容量瓶未经干燥使用。 其中引起所配溶液浓度偏高的有______________(填序号,下同),偏低的有______________,无影响的有_______________________________。
(3)下列操作中,容量瓶所不具备的功能有________________。
A.配制一定体积准确浓度的标准溶液 B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体 D.准确稀释某一浓度的溶液
E.用来加热溶解固体溶质
(4)某同学改用固体Na2CO3配制上述Na2CO3溶液的过程如图所示:

你认为该同学的错误步骤有_________________。
A.1处 B.2处 C.3处 D.4处
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在2 L密闭容器中投入一定量的A、B,发生反应3A(g)+bB(g) ![]() cC(g)。12 s时达到平衡,生成C的物质的量为0.8 mol,反应过程如图所示。下列说法正确的是
cC(g)。12 s时达到平衡,生成C的物质的量为0.8 mol,反应过程如图所示。下列说法正确的是

A. 前12 s内,A的平均反应速率为0. 025 mol L-1 s-1
B. 12 s后,A的消耗速率等于B的生成速率
C. 化学计量数之比b:c==1:2
D. 反应开始到12 s,A的转化率为70%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“常见无机物”,主要是指的铝、铁、硫、氯四种元素的单质及化合物。完成下列填空:
(1)四种元素原子的半径大小Fe >______>______>______
(2)铝原子核外电子排布式_________________________,有_________种不同能量级的电子;铝热剂的成分是铝粉与氧化铁的混合物;写出铝热反应的化学方程式____________________
(3)工业上用氯气和__________制取漂粉精;吸收多余氯气的试剂是______________。
(4)硫磺粉末与铁粉混合加热,写出该反应的化学反应方程式并标出电子转移的方向和数目______________________________________________________。
(5)硫的非金属性________于氯(选填“强”、“弱”),用一个事实证明______________________,
再从原子结构的知识加以解释____________________________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水提溴一般需要经过浓缩、氧化和提取三个步骤。下列对操作步骤描述错误的是
A. 浓缩的原理是蒸发结晶 B. 氧化时通入氯气
C. 提取时利用Br2易挥发 D. 提取时用CCl4萃取
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重金属元素铬的毒性较大,含铬废水需经处理达标后才能排放。
Ⅰ、某工业废水中主要含有Cr3+,同时还含有少量的Fe3+、Al3+、Ca2+和Mg2+等,且酸性较强。为回收利用,通常采用如下流程处理:

注:部分阳离子常温下以氢氧化物形式完全沉淀时溶液的pH见下表。
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Mg(OH)2 | Al(OH)3 | Cr(OH)3 |
pH | 3.7 | 9.6 | 11.1 | 8 | 9(>9溶解) |
(1)氧化过程中可代替H2O2加入的试剂是________(填序号)。
A.Na2O2 B.HNO3 C.FeCl3 D.KMnO4
(2)加入NaOH溶液调整溶液pH=8时,除去的离子是________;已知钠离子交换树脂的原理:Mn++nNaR—→MRn+nNa+,此步操作被交换除去的杂质离子是__________。
A.Fe3+ B.Al3+ C.Ca2+ D.Mg2+
(3)还原过程中,每消耗0.8 mol Cr2O72-转移4.8 mol e-,该反应离子方程式为______________。
Ⅱ、酸性条件下,六价铬主要以Cr2O72-形式存在,工业上常用电解法处理含Cr2O72-的废水;该法用Fe作电极电解含Cr2O72-的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3溶液。
(4)电解时能否用Cu电极来代替Fe电极?________(填“能”或“不能”),理由是____________________。
(5)电解时阳极附近溶液中Cr2O72-转化为Cr3+的离子方程式为__________________________。
(6)常温下,Cr(OH)3的溶度积Ksp=1×10-32,溶液的pH应为____时才能使c(Cr3+)降至10-5 mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定量的FeO、Fe、Fe2O3的混合物中加入100 mL 1mol/L盐酸,恰好使混合物完全溶解,放出112 mL(标准状况)的气体,在所得溶液中加入KSCN溶液无血红色出现。若用足量的CO在高温下还原相同质量的此混合物,能得到铁的质量为
A. 2.8g B. 5.6g C. 8.4g D. 无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸苯甲酯对花香和果香的香气有提升作用,故常用于化妆品工业和食品工业。乙酸苯甲酯可以用下面的设计方案合成。
(1)A结构简式为____________;B的官能团名称为________________;
(2)反应③的化学方程式为______________________________;
(3)D有很多同分异构体,苯环上只有一个取代基且属于酯类化合物的同分异构体共5个,已知其中3个的结构简式是:

请写出另外两个同分异构体的结构简式________________、___________________;
(4)C的同分异构体E,能与浓溴水反应生成白色沉淀,其核磁共振氢谱有4组吸收峰,E的结构简式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】测定有机化合物中碳和氢的组成常用燃烧分析法,下图是德国化学家李比希测定有机物组成的装置,氧化铜作催化剂,在750 ℃左右使有机物在氧气流中全部氧化为CO2和H2O,用含有固体氢氧化钠和氯化钙的吸收管分别吸收CO2和H2O。
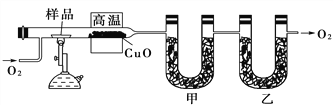
试回答下列问题:
(1)甲装置中盛放的是________,甲、乙中的吸收剂能否颠倒?并请说明理由:_________________________________________________。
(2)实验开始时,要先通入氧气一会儿,然后再加热,为什么?
_________________________________________________________。
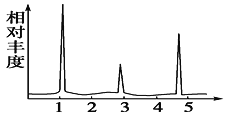
有机物A的核磁
共振氢谱图
(3)将4.6 g有机物A进行实验,测得生成5.4 g H2O和8.8 g CO2,则该物质中各元素的原子个数比是________。
(4)经测定,有机物A的核磁共振氢谱示意图如图,则A的结构简式为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com