
【题目】“常见无机物”,主要是指的铝、铁、硫、氯四种元素的单质及化合物。完成下列填空:
(1)四种元素原子的半径大小Fe >______>______>______
(2)铝原子核外电子排布式_________________________,有_________种不同能量级的电子;铝热剂的成分是铝粉与氧化铁的混合物;写出铝热反应的化学方程式____________________
(3)工业上用氯气和__________制取漂粉精;吸收多余氯气的试剂是______________。
(4)硫磺粉末与铁粉混合加热,写出该反应的化学反应方程式并标出电子转移的方向和数目______________________________________________________。
(5)硫的非金属性________于氯(选填“强”、“弱”),用一个事实证明______________________,
再从原子结构的知识加以解释____________________________________________________.
【答案】 Al S Cl 1s22s22P63s23P1 5 2Al+Fe2O3 ![]() 2 Fe + Al2O3 消石灰或熟石灰 氢氧化钠溶液
2 Fe + Al2O3 消石灰或熟石灰 氢氧化钠溶液 ![]() 弱 氯化氢比硫化氢稳定,氯气与氢气点燃即可燃烧或爆咋,而硫磺与氢气加热还较难反应且可逆,高氯酸的酸性强于硫酸等(合理即给分) S与Cl二者电子层数相同,核外电子数增多,原子半径逐渐减小,原子核对外层电子的吸引力增强,故得电子能力依次增强,非金属性增强。
弱 氯化氢比硫化氢稳定,氯气与氢气点燃即可燃烧或爆咋,而硫磺与氢气加热还较难反应且可逆,高氯酸的酸性强于硫酸等(合理即给分) S与Cl二者电子层数相同,核外电子数增多,原子半径逐渐减小,原子核对外层电子的吸引力增强,故得电子能力依次增强,非金属性增强。
【解析】(1)同周期自左向右原子半径逐渐减小,同主族自上而下原子半径逐渐增大,则四种元素原子的半径大小Fe>Al>S>Cl;(2)铝原子的质子数是13,核外电子排布式为1s22s22p63s23p1,有5种不同能量级的电子;铝热剂的成分是铝粉与氧化铁的混合物,反应的化学方程式为2Al+Fe2O3![]() 2Fe+Al2O3;(3)工业上用氯气和消石灰或熟石灰制取漂粉精;吸收多余氯气的试剂是氢氧化钠溶液;(4)硫磺粉末与铁粉混合加热生成硫化亚铁,铁失去电子,方程式为
2Fe+Al2O3;(3)工业上用氯气和消石灰或熟石灰制取漂粉精;吸收多余氯气的试剂是氢氧化钠溶液;(4)硫磺粉末与铁粉混合加热生成硫化亚铁,铁失去电子,方程式为![]() 。(5)同周期自左向右非金属性逐渐增强,因此硫的非金属性弱于氯,这是由于S与Cl二者电子层数相同,核外电子数增多,原子半径逐渐减小,原子核对外层电子的吸引力增强,故得电子能力依次增强,非金属性增强。能说明该事实有氯化氢比硫化氢稳定,氯气与氢气点燃即可燃烧或爆咋,而硫磺与氢气加热还较难反应且可逆,高氯酸的酸性强于硫酸等。
。(5)同周期自左向右非金属性逐渐增强,因此硫的非金属性弱于氯,这是由于S与Cl二者电子层数相同,核外电子数增多,原子半径逐渐减小,原子核对外层电子的吸引力增强,故得电子能力依次增强,非金属性增强。能说明该事实有氯化氢比硫化氢稳定,氯气与氢气点燃即可燃烧或爆咋,而硫磺与氢气加热还较难反应且可逆,高氯酸的酸性强于硫酸等。


科目:高中化学 来源: 题型:
【题目】重铬酸钾(K2Cr2O7)是一种强氧化剂,在实验室和工业中都有很广泛的应用。同时,由于其具有致癌作用,也是环境污染物之一,必须进行处理。工业上通常以铬铁矿(主要成分为FeOCr2O3,另外还含有SiO2、Al2O3等杂质)为原料制备重铬酸钾,主要流程如下图所示:
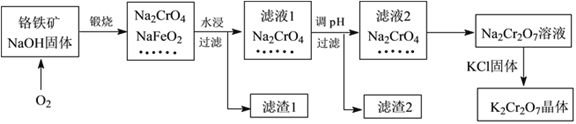
已知:①NaFeO2遇水强烈水解,生成红褐色物质;
②2CrO42—(黄色)+2H+![]() Cr2O72—(橙色)+H2O
Cr2O72—(橙色)+H2O
请回答下列问题:
Ⅰ.(1)滤液1的溶质除Na2CrO4、Na2SiO3外,还含有(填化学式)_________________;
(2)由滤液2转化为Na2Cr2O7溶液过程中,能说明反应达平衡状态的是_______(填字母代号);
a.溶液的颜色不变
b.v (CrO42—)= 2v (Cr2O72—)
c.Cr2O72—和CrO42—的浓度相同
(3)向Na2Cr2O7溶液中加入KCl固体,获得K2Cr2O7晶体的操作依次是:加热浓缩、______________、过滤、洗涤、干燥。
Ⅱ.工业废水中常含有一定量的Cr2O72—和CrO42—,常用还原沉淀法处理。该方法的工艺流程为:
![]()
(4)请写出Cr2O72―与FeSO4溶液在酸性条件下反应的离子方程式___________________;
(5)已知常温下,Cr(OH)3的溶度积Ksp=10-32,要使第步过程中c(Cr3+)降至10-5mol/L,溶液的pH应调至__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】正在研制的一种“高容量、低成本”锂-铜空气燃料电池,该电池通过一种复杂的铜腐蚀现象产生电力,其中放电过程2Li+Cu2O+H2O=2Cu+2Li++20H-,下列说法不正确的是

A. 放电一段时间后右侧水溶液pH升高
B. 整个反应过程中,铜相当于催化剂
C. 通空气时,铜被腐蚀,表面产生CuO
D. 放电时,正极的电极反应式为 Cu2O+H2O+2e-=Cu+2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的反应,属于同一反应类型的是
A.由溴丙烷水解制丙醇;由丙烯与水反应制丙醇
B.由甲苯硝化制对硝基甲苯;由甲苯氧化制苯甲酸
C.由氯代环己烷消去制环己烯;由丙烯加溴制1,2二溴丙烷
D.由乙酸和乙醇制乙酸乙酯;由苯甲酸乙酯水解制苯甲酸和乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于二氧化碳和二氧化硅说法中正确的是( )
A. 都可以与水化合生成对应酸
B. 都可以与氢氟酸反应生成气体
C. 都可以跟氢氧化钠溶液反应生成盐和水
D. 都可以形成空间立体网状结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阅读下表中短周期主族元素的相关信息。
元素 | 相关信息 |
A | A的单质能与冷水剧烈反应,得到强喊性溶液 |
B | B的原子最外层电子数是其内层电子数的3倍 |
C | 在第三周期元素中,C的简单离子半径最小 |
D | A、B、D组成的36电子的化合物X是家用消毒剂的主要成分 |
E | 所有有机物中都含有E元素 |
(1) E在元素周期表中的位置是_____________________。
(2) X的化学式为____________________
(3) A、B、C三种元素形成的简单离子半径由大到小的顺序为________________ (用离子符号表示)。
(4)A的单质在真空高压下能与由元素D、E组成的化合物ED4反应生成两种固体物质,其中一种是自然界中硬度最大的物质,此反应在科学上有“稻草变黄金”的美称。写出该反应的化学方程式:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 做衣服的棉、麻、蚕丝的主要成分都是纤维素
B. 油脂在碱性条件下的水解为皂化反应
C. 石油的分馏和煤的干馏都是物理变化
D. 饱和Na2SO4、CuSO4溶液均可用于蛋白质的盐析
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在无色强酸性溶液中,下列各组离子能大量共存的是
A. K+、Fe3+、SO42﹣、NO3﹣ B. Na+、K+、NH4+、Cl﹣
C. Ag+、Na+、NO3﹣、Cl﹣ D. K+、Na+、ClO﹣、CO32﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯分子并不具有碳碳单键和碳碳双键的简单交替结构,可作为证据的事实有( C )
①苯的间位二元取代物只有一种 ②苯的邻位二元取代物只有一种 ③苯不能使酸性KMnO4溶液褪色 ④苯能在一定条件下与氢气反应生成环己烷 ⑤苯在FeBr3存在的条件下同液溴发生取代反应而不是加成反应 ⑥苯不能使溴水因发生化学反应而褪色
A. ①②③⑥ B. ③④⑤ C. ②③⑤⑥ D. ②③⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com