
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:
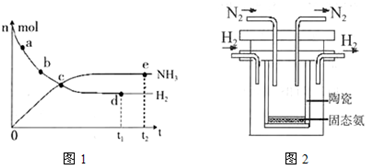
查看答案和解析>>
科目:高中化学 来源:海南省嘉积中学2010-2011学年高一教学质量监测化学试题(二) 题型:021
|
下列叙述正确的是 ①2 mol铁原子 ②1 mol Fe3+ ③0.5 mol氧 ④0.5 mol氮气 ⑤氨的摩尔质量是17 g | |
A. |
①③④ |
B. |
①②④⑤ |
C. |
①②④ |
D. |
都正确 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com