
【题目】目前我国研制的稀土催化剂催化转化汽车尾气示意图如下:
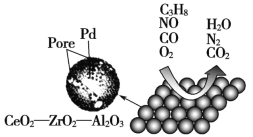
(1)Zr原子序数为40,价电子排布式为4d25s2,它在周期表中的位置是_______________。
(2)图中互为等电子体的两种气体分子是_____________。
(3)C3H8中所有碳原子的杂化方式是___________。
(4)图中属于非极性的气体分子是_______________________。
Fe、Mn元素的部分电离能数据列于下表中
元素 | Fe | Mn | |
电离能(kJ·mol-1) | I1 | 759 | 717 |
I2 | 1561 | 1509 | |
I3 | 2957 | 3248 | |
(5)从上表两元素部分电离能数据比较的可知,气态Mn2+再失去一下电子比气态Fe2+再夫去一个电子难,原因是_____________。
(6)CO与Ni可生成羰基镍[Ni(CO)4],已知其中镍的化合价为0,镍原子在基态时核外电子排式为_____________,[Ni(CO)4]的配体是_________,配位原子是__________。
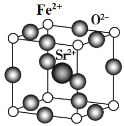
(7)为了节省贵金属并降低成本,也常用钙钛矿型复合氧化物作为催化剂。一种复合氧化物结构如图所示,则与每个Sr2+紧邻的O2-有______个。
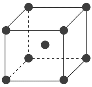
(8)与Zr相邻的41号元素Nb金属的晶格类型为体心立方晶格,原子半径为apm,相对原子质量为b,阿伏加德罗常数为NA,试计算晶体铌的密度为______________g·cm-3(用来a、b、NA表示计算结果)。
【答案】第五周期ⅣB族 N2、CO sp3 N2、O2、CO2 Mn2+转为化Mn3+时,3d能级由较稳定的3d5半充满状态转变为不稳定的3d4状态 1s22s22p63s23p63d84s2或[Ar] 3d84s2 CO C 12 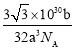
【解析】
(1)根据原子序数和价电子排布式分析其在元素周期表中的位置;
(2)原子总数相同,价电子总数也相同的分子、离子或基团为等电子体;
(3)根据C3H8中碳原子的成键方式判断杂化方式;
(4)正负电荷中心重合的分子为非极性分子;
(5)根据Mn2+和Fe2+的核外电子排布分析;
(6)镍元素为28号元素;配合物中一般由金属离子提供空轨道,非金属原子提供孤对电子;
(8)根据原子半径计算晶胞棱长,得到晶胞体积,根据均摊法计算晶胞中原子数目,计算质量,再根据![]() 计算密度。
计算密度。
(1)Zr原子序数为40,价电子排布式为4d25s2,最高能层为5,位于周期表第5周期,价电子数为4,位于第4纵列,所以位于第ⅣB族,即Zr位于周期表第5周期ⅣB族;
(2)N2和CO原子总数相同,价电子总数均为10,二者互为等电子体;
(3)C3H8分子中每个C原子含有4个σ键,所以每个C原子价层电子对数是4,则C原子采用sp3杂化;
(4)O2和N2是以非极性键结合的双原子一定为非极性分子;CO2中含有极性键,空间构型为直线形,结构对称,分子中正负电荷中心重叠,为非极性分子;
(5)由Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态转为不稳定的3d4状态需要的能量较多;而Fe2+到Fe3+时,3d能级由不稳定的3d6到稳定的3d5半充满状态,需要的能量相对要少;
(6)镍元素为28号元素,根据核外电子排布规律可知基态Ni原子的核外电子排布式为1s22s22p63s23p63d84s2或[Ar] 3d84s2;[Ni(CO)4]的配体是CO,虽然C和O原子都有孤电子对,但C的电负性较小更容易给出电子,所以配位原子为C;
(7)根据晶胞结构示意图可知,位于棱心上的12个O2-与Sr2+紧邻;
(8)体心立方堆积中体对角线上的三个原子相切,设晶胞棱长为x,则有![]() x=4a,所以x=
x=4a,所以x=![]() apm,则晶胞的体积V=
apm,则晶胞的体积V=![]() 3pm3=
3pm3=![]() 3×10-30cm3;根据均摊法,晶胞中所含Nb原子的个数为
3×10-30cm3;根据均摊法,晶胞中所含Nb原子的个数为![]() =2,所以晶胞的质量m=
=2,所以晶胞的质量m=![]() g,所以晶胞的密度为
g,所以晶胞的密度为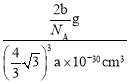 =
=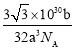 g·cm-3。
g·cm-3。


科目:高中化学 来源: 题型:
【题目】(1)按要求填空
①4.8gO3和0.2molCH4,在同温同压下的体积之比是____。②同温同压下,NH3和H2S气体的密度比是___;③同温同体积下,同质量的NH3和H2S气体的压强之比是___。
(2)写出下列物质在水中的电离方程式:
NaHSO4:___
H2SO4:___
NaHCO3:___
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】试根据氧化还原反应:2FeCl3+Cu=2FeCl2+CuCl2设计原电池,并画出装置图________________,指出电解质溶液是________________,负极是________________,电极反应式为__________________,正极是___________,电极反应式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1,2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=-1452 kJ·mol-1,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,下列说法正确的是
A.H2(g)的燃烧热为571.6 kJ·mol-1
B.同质量的H2(g)和CH3OH(l)完全燃烧,H2(g)放出的热量多
C.![]() H2SO4(aq)+
H2SO4(aq)+![]() Ba(OH)2(aq)=
Ba(OH)2(aq)=![]() BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1
BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1
D.3H2(g)+CO2(g)=CH3OH(l)+H2O(l) ΔH=+135.9 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1200℃时,天然气脱硫工艺中会发生下列反应
①H2S(g)+![]() O2(g)=SO2(g)+H2O(g) ΔH1 ②2H2S(g)+SO2(g)=
O2(g)=SO2(g)+H2O(g) ΔH1 ②2H2S(g)+SO2(g)=![]() S2(g)+2H2O(g) ΔH2
S2(g)+2H2O(g) ΔH2
③H2S(g)+![]() O2(g)=S(g)+H2O(g) ΔH3 ④2S(g)=S2(g) ΔH4
O2(g)=S(g)+H2O(g) ΔH3 ④2S(g)=S2(g) ΔH4
则ΔH4的正确表达式为
A.ΔH4=![]() (ΔH1+ΔH2-3ΔH3)B.ΔH4=
(ΔH1+ΔH2-3ΔH3)B.ΔH4=![]() (3ΔH3-ΔH1-ΔH2)
(3ΔH3-ΔH1-ΔH2)
C.ΔH4=![]() (ΔH1+ΔH2-3ΔH3)D.ΔH4=
(ΔH1+ΔH2-3ΔH3)D.ΔH4=![]() (ΔH1-ΔH2-3ΔH3)
(ΔH1-ΔH2-3ΔH3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将3mol A与3mol B混合于3L的密闭容器中,发生如下反应:2A(g)+3B(g)![]() 2C(g)+nD(g),2s后达平衡A的转化率为50%,测得v(D)=0.25molL-1s-1,下列推断正确的是( )
2C(g)+nD(g),2s后达平衡A的转化率为50%,测得v(D)=0.25molL-1s-1,下列推断正确的是( )
A.v(B)=0.25molL-1s-1B.C的体积分数为30%
C.B的转化率为25%D.n=2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某些共价键的键能数据如表(单位:kJmol-1):
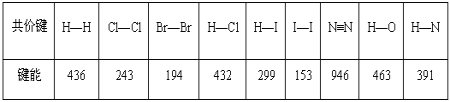
(1)把1mol Cl2分解为气态原子时,需要___(填“吸收”或“放出”)243kJ能量。
(2)由表中所列化学键形成的单质分子中,最稳定的是___;形成的化合物分子中最不稳定的是___。
(3)发射火箭时用气态肼(N2H4)作燃料,二氧化氮作氧化剂,两者反应生成氮气和气态水。已知32gN2H4(g)完全发生上述反应放出568kJ的热量,热化学方程式是:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】84消毒液、酒精、过氧乙酸等消毒剂在抗击新型冠状病毒肺炎疫情中起到重要作用。回答下列问题:
Ⅰ.84消毒液是北京第一传染病医院(现北京地坛医院)于1984年研制的一种消毒液,主要成分为受热易分解的次氯酸钠(NaClO)。某实验小组用如图装置制备84消毒液。
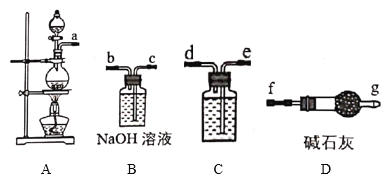
(1)A中发生反应的离子方程式为___。
(2)C中盛装试剂为__,仪器的连接顺序为a→__。
(3)制备84消毒液时,若Cl2与NaOH溶液反应温度过高,NaClO的产率将__(填“增大”“减小”或“不变”)。
Ⅱ.过氧乙酸(CH3COOOH)是无色液体,易溶于水,有强烈刺激性气味,有腐蚀性,对人的眼睛、皮肤、黏膜、上呼吸道等有强烈刺激作用,易分解,易爆炸。
(4)贮存和运输CH3COOOH时要注意的事项是__。
(5)消毒过程中需将200mL20%的过氧乙酸(密度为1.02g·cm-3)稀释为0.5%的过氧乙酸,则需加入水的体积为__![]() 。
。
(6)CH3COOOH可用H2O2和CH3COOH制备,其化学方程式为___。
(7)制备CH3COOOH过程中总会残留少量H2O2,因此CH3COOOH在使用过程中需要准确标定原液的浓度。取CH3COOOH样品![]() ,标定步骤如下:
,标定步骤如下:
a.用KMnO4标准溶液滴定H2O2;
b.当达到终点时加入足量KI溶液,发生反应:2KI+H2SO4+CH3COOOH=2KHSO4+CH3COOH+H2O+I2;
c.用1.500mol·L-1Na2S2O3标准溶液滴定生成的I2,发生反应:I2+2Na2S2O3=2NaI+Na2S4O6,消耗Na2S2O3溶液20.00mL。
测得样品中CH3COOOH的质量分数为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
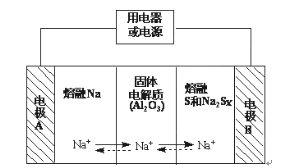
【题目】Ⅰ、钠硫电池作为一种新型储能电池,其应用逐渐得到重视和发展。钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如图所示:
物质 | Na | S | Al2O3 |
熔点/℃ | 97.8 | 115 | 2050 |
沸点/℃ | 892 | 444.6 | 2980 |
(1)请判断该电池工作的适宜温度应控制在____范围内(填字母序号)。
A.常温 B.60℃~ 100℃ C.200℃~350℃ D.2000℃~3000℃
(2)放电时,电极A为___极。
(3)放电时,内电路中Na+的移动方向为___(填“从A到B”或“从B到A”)。
(4)充电时,总反应为Na2Sx=2Na+xS(3<x<5),则阳极的电极反应式为___。
Ⅱ、用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如图所示。(电极材料为石墨)
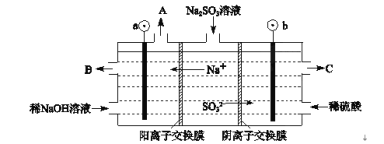
(1)图中a极要连接电源的(填“正”或“负”)___极,C口流出的物质是___。
(2)SO32-放电的电极反应式为____。
(3)电解过程中阴极区碱性明显增强,请结合电极方程式解释原因___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com