
【题目】有![]() 、CH3CH2OH、CH3CH2Br、NH4Cl四种无色液体,只有一种试剂就能把它们鉴别开,这种试剂是( )
、CH3CH2OH、CH3CH2Br、NH4Cl四种无色液体,只有一种试剂就能把它们鉴别开,这种试剂是( )
A.溴水B.NaOH溶液C.Na2SO4溶液D.KMnO4溶液
【答案】BD
【解析】
苯和CH3CH2Br都不溶于水,但苯的密度比水小,CH3CH2Br的密度比水大,CH3CH2Br可在碱性条件下水解,生成CH3CH2OH,CH3CH2OH和水混溶,NH4Cl溶液中加入NaOH,生成具有刺激性气味的氨气,以此解答该题。
A.溴水与CH3CH2OH、NH4Cl溶液不反应,无明显现象,不能鉴别,故A不选;
B.苯不溶于水,密度比水小,乙醇和水混溶,CH3CH2Br可在碱性条件下水解,生成CH3CH2OH,油状液体逐渐消失,NH4Cl溶液中加入NaOH,生成具有刺激性气味的氨气,可鉴别,故B选;
C.Na2SO4溶液不能鉴别CH3CH2OH、NH4Cl溶液,故C不选;
D.加入高锰酸钾,可氧化乙醇而褪色,苯与高锰酸钾不反应,密度比水小,有机层在上层,CH3CH2Br密度比水大,有机层在下层,氯化铵与高锰酸钾溶液不分层,可鉴别,故D选;
故答案选BD。


科目:高中化学 来源: 题型:
【题目】燃烧0.1 mol某有机物得0.2 mol CO2和0.3 mol H2O,由此得出的结论不正确的是( )
A. 该有机物分子的结构简式为CH3—CH3
B. 该有机物中碳、氢元素原子数目之比为1∶3
C. 该有机物分子中不可能含有![]() 双键
双键
D. 该有机物分子中可能含有氧原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】立方烷结构为立方体,分子式为C8H8,其熔点比相同碳原子的辛烷高,立方烷的结构简式如图所示。下列有关立方烷的说法正确的是( )

A.其一氯代物只有1种,二氯代物有2种
B.常温常压下为气体
C.与乙苯(结构简式为![]() )是同分异构体
)是同分异构体
D.与苯的含碳质量分数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家设计二氧化碳熔盐捕获及电化学转化装置,其示意图如下:

下列说法不正确的是
A. b为电源的正极
B. ①②中,捕获CO2时碳元素的化合价发生了变化
C. a极的电极反应式为2C2O52 4e == 4CO2 + O2
D. 上述装置存在反应:CO2 ===== C + O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】蒽(![]() )与苯炔(
)与苯炔(![]() )反应生成化合物X(立体对称图形),如图所示:
)反应生成化合物X(立体对称图形),如图所示:
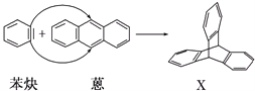
(1)蒽与X都属于__;
a.环烃 b.烷烃 c.芳香烃
(2)苯炔的分子式为__,苯炔不具有的性质是__;
a.能溶于水 b.能发生氧化反应 c.能发生加成反应 d.常温常压下为气体
(3)下列属于苯的同系物的是__(填字母符号);
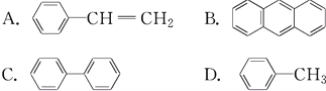
(4)能发生加成反应,也能发生取代反应,同时能使溴水因反应褪色,也能使酸性高锰酸钾溶液褪色的是__。
A.![]() B.C6H14 C.
B.C6H14 C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.18g18O3中含有的中子数为8NA
B.0.1mol·L-1Na2CO3溶液中,所含阴离子总数大于0.1NA
C.7.8gNa2O2参与反应,转移的电子数一定为0.1NA
D.标准状况下,22.4LCO2和SO2的混合气体中含有的氧原子数目为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中烧杯里盛的是海水,铁被腐蚀由快到慢的顺序是( )
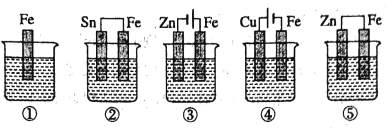
A.③>②>①>⑤>④B.④>②>①>③>⑤C.③>②>④>⑤>①D.④>⑤>②>③>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组热化学方程式中,化学反应的ΔH前者大于后者的是( )
①C(s)+O2(g)= CO2(g)ΔH1;C(s)+ ![]() O2(g)= CO(g)ΔH2
O2(g)= CO(g)ΔH2
②S(s)+O2(g)= SO2(g)ΔH3;S(g)+O2(g)=SO2(g)ΔH4
③H2(g)+ ![]() O2(g)=H2O(l)ΔH5;2H2(g)+O2(g)= 2H2O(l)ΔH6
O2(g)=H2O(l)ΔH5;2H2(g)+O2(g)= 2H2O(l)ΔH6
④CaCO3(s)= CaO(s)+CO2(g)ΔH7;CaO(s)+H2O(l)= Ca(OH)2(s)ΔH8
A.①B.④C.②③④D.①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废弃锂离子电池的资源化处理日益重要。从废旧磷酸铁锂电池的正极材料(含LiFePO4、石墨粉和铝箔等)中综合回收锂、铁和磷等的工艺流程如图所示:
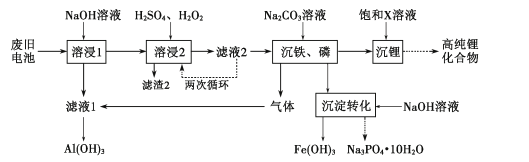
有关数据:25℃时,Ksp(FePO4)=1.3×10-22、Ksp[Fe(OH)3]=2.6×10-39。
回答下列问题:
(1)“溶浸1”中铝溶解的化学方程式为___。
(2)完成“溶浸2”反应的离子方程式___:
![]() LiFePO4+
LiFePO4+![]() H2O2+
H2O2+![]() =
=![]() Li++
Li++![]() +
+![]() H2PO4-+
H2PO4-+![]() H2O
H2O
(3)“滤渣2”的主要成分是___。
(4)“滤液2”循环两次的目的是___。
(5)“沉铁、磷”时,析出FePO4沉淀,反应的离子方程式为__。实验中,铁、磷的沉淀率结果如图所示。碳酸钠浓度大于30%后,铁沉淀率仍然升高,磷沉淀率明显降低,其可能原因是___。
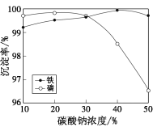
(6)“沉淀转化”反应:FePO4+3OH-Fe(OH)3+PO43-。用此反应的化学平衡常数说明转化能否完全___?
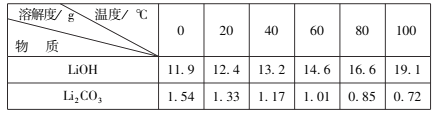
(7)为了充分沉淀,“沉锂”时所用的X和适宜温度是___(填标号)。
A.NaOH20-40℃ B.NaOH80-100℃
C.Na2CO320-40℃ D.Na2CO360-80℃
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com