
 2Q(g)+nR(g)达到平衡时测得 X的转化率为25%,此时混合气体的体积为6.5L。则该反应方程式中的n值是( )
2Q(g)+nR(g)达到平衡时测得 X的转化率为25%,此时混合气体的体积为6.5L。则该反应方程式中的n值是( )| A.3 | B.5 | C.6 | D.8 |
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案科目:高中化学 来源:不详 题型:单选题
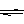 2SO3(g);△H=-197KJ/mol。在相同的温度和压强下,向密闭容器中通入2molSO2和1molO2,达到平衡时放出热量Q1,向另一个体积相同的容器中通入1molSO2、0.5molO2和1molSO3,达到平衡时放出热量Q2。则下列关系式正确的是( )
2SO3(g);△H=-197KJ/mol。在相同的温度和压强下,向密闭容器中通入2molSO2和1molO2,达到平衡时放出热量Q1,向另一个体积相同的容器中通入1molSO2、0.5molO2和1molSO3,达到平衡时放出热量Q2。则下列关系式正确的是( )| A.Q1=Q2=197KJ | B.Q1<Q2<197KJ | C.Q2<Q1<197KJ | D.Q1=Q2<197KJ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2HBr(g)达到平衡的标志是
2HBr(g)达到平衡的标志是| A.断裂1 mol H-H键的同时生成2 mol H-Br键 |
| B.单位时间内消耗1 mol H2,同时生成1 mol Br2 |
| C.H2、Br2、HBr的分子数之比为1∶1∶2 |
| D.混合气体的压强不再改变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 cC+Q在某温度下的平衡常数为K(K≠1),反应热为Q。保持温度不变,将方程式的书写作如下改变,则Q和K数值的相应变化为
cC+Q在某温度下的平衡常数为K(K≠1),反应热为Q。保持温度不变,将方程式的书写作如下改变,则Q和K数值的相应变化为A.写成2aA+2bB 2cC,Q值、K值均扩大了一倍 2cC,Q值、K值均扩大了一倍 |
B.写成2aA+2bB 2cC,Q值扩大了一倍,K值保持不变 2cC,Q值扩大了一倍,K值保持不变 |
C.写成cC aA+bB,Q值、K值变为原来的相反数 aA+bB,Q值、K值变为原来的相反数 |
D.写成cC aA+bB,Q值变为原来的相反数,K值变为倒数 aA+bB,Q值变为原来的相反数,K值变为倒数 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 C(g)
C(g) 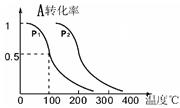
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2AB(气),达到平衡的标志是
2AB(气),达到平衡的标志是| A.容器的总压强不随时间而变化 |
| B.单位时间内有n molA2生成的同时有n molB2生成 |
| C.单位时间内有n molB2发生反应的同时有n molAB分解 |
| D.单位时间内生成n molA2同时就有2n molAB生成 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
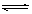 2C(g)在一个密闭容器中达到平衡时,测得c(A2)=0.5mol·L-1,c(B2)=0.1mol·L-1,c(C)=1.6mol·L-1。若
2C(g)在一个密闭容器中达到平衡时,测得c(A2)=0.5mol·L-1,c(B2)=0.1mol·L-1,c(C)=1.6mol·L-1。若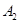 、
、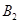 、C的起始浓度分别为a mol·L-1、b mol·L-1、g mol·L-1请确定:
、C的起始浓度分别为a mol·L-1、b mol·L-1、g mol·L-1请确定:查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.开启啤酒瓶后,瓶中马上泛起大量泡沫 |
| B.H2、I2、HI混合气体加压后颜色变深 |
| C.红棕色的NO2加压后颜色先变深再变浅 |
| D.工业上生产硫酸的过程中使用过量的空气,以提高二氧化硫的利用率 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 Fe2O3(s)+3CO(g)
Fe2O3(s)+3CO(g)| A.升高温度 | B.增大压强 |
| C.充入一定量CO | D.再加一些铁粉 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com