
| A、沉淀中只有Fe(OH)3 |
| B、沉淀中有Fe(OH)3和Fe(OH)2 |
| C、滤液c(Fe3+)=4.0×10-8mol/L |
| D、向滤液中滴加FeCl2溶液,无沉淀产生 |


 金钥匙试卷系列答案
金钥匙试卷系列答案科目:高中化学 来源: 题型:
| 拆开化学键 | 形成化学键 | 则上述反应中能量变化是多少(列出计算式)?是放热还是吸热? |
| 2mol H2中的化学键 | 4mol H-O键 | |
| 1mol O2中的化学键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
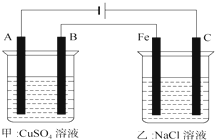 如图为相互串联的甲、乙两个电解池(电极A、B、C都是惰性电极),请回答:
如图为相互串联的甲、乙两个电解池(电极A、B、C都是惰性电极),请回答:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶于水后得到的溶液能导电的物质 |
| B、BaSO4、AgCl是难溶物,但它们是电解质 |
| C、盐酸、氨水、CO2都是电解质 |
| D、在水溶液中或熔融状态下能导电的化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、最后所得溶液的物质的量浓度是0.33mol/L |
| B、通过装置①②后气体体积仍为6.72L |
| C、通过装置③后所得气体呈红棕色 |
| D、集气瓶中收集到0.025mol O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、最外层只有1个电子的元素一定是金属元素 |
| B、最外层只有2个电子的元素一定是金属元素 |
| C、原子核外各层电子数相等的元素不一定是金属元素 |
| D、核电荷数为17的元素的原子在化学反应中容易得到1个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径:A<B<C<D |
| B、B元素在周期表中的位置为第二周期第 VIA族 |
| C、D元素最高价氧化物的水化物难溶于水 |
| D、C、D、A、B四种元素的最高化合价依次升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、升高温度正反应速率加快,逆反应速率减慢 |
| B、0.1mol A2和0.2mol B2反应达到平衡时生成0.2mol AB2 |
| C、达平衡后,升高温度,B的转化率增大 |
| D、催化剂可同等程度地改变正、逆反应速率 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com