
| 装置 | 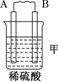 | 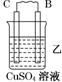 | 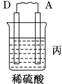 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
分析 甲装置中,二价金属A不断溶解说明该装置构成了原电池,且A失电子发生氧化反应而作负极,B作正极;乙中C的质量增加,说明C上铜离子得电子发生还原反应,则C作原电池正极,B作负极;丙装置中A上有气体产生,说明A上氢离子得电子发生还原反应,则A作原电池正极,D作负极,作原电池负极的金属活动性大于作正极金属,所以金属活动性强弱顺序是:D>A>B>C.
解答 解:(1)该装置中,二价金属A不断溶解说明A失电子发生氧化反应生成金属阳离子进入溶液而作负极,所以负极电极反应式为A-2e-═A2+,
故答案为:A-2e-═A2+;
(2)乙装置中,C的质量增加说明C电极上铜离子得电子发生还原反应,则C作正极,电极反应式为Cu2++2e-═Cu,若电路中转移6.02×1022个e-,所以转移电子的物质的量为:0.1mol,生成铜0.05mol,质量为0.05mol×64g/mol=3.2g,故答案为:3.2g;
(3)丙装置中A上有气体产生,说明A上氢离子得电子发生还原反应而作正极,D作负极,正极上氢离子逐渐析出而导致氢离子浓度逐渐减小,则溶液的pH逐渐增大,故答案为:变大;
(4)通过以上分析知,四种金属活动性强弱顺序是D>A>B>C,故答案为:D>A>B>C.
点评 本题考查了原电池原理,根据原电池电极上得失电子来判断正负极,一般来说,作原电池负极的金属金属活动性顺序强,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 醋酸溶液与氢氧化钠溶液反应:CH3COOH+OH-═CH3COO-+H2O | |
| B. | 碳酸氢钠与盐酸反应:CO32-+2H+═H2O+CO2↑ | |
| C. | 铁与稀硫酸反应:Fe+2H+═Fe3++H2↑ | |
| D. | 钠与水反应:Na+2H2O═Na++2OH-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
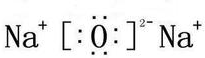 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 其单质在常温下跟水的反应不如钠剧烈 | |
| B. | 其原子半径比钾离子半径小 | |
| C. | In是第5周期ⅠB族元素 | |
| D. | 其氢氧化物能使氢氧化铝溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
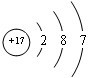 ;B的最高价氧化物电子式
;B的最高价氧化物电子式
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | VA | VIA | ⅥA | O族 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | ⑩ |
 ,该化合物属于离子(填“共价”或“离子”)化合物.
,该化合物属于离子(填“共价”或“离子”)化合物. ,该化合物是由极性(填“极性”或“非极性”)键形成的.
,该化合物是由极性(填“极性”或“非极性”)键形成的.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 此法对环境不会造成任何污染 | |
| B. | 沉降、过滤、洗涤沉淀物操作中既有物理变化也有化学变化 | |
| C. | 若提取12 kg Mg,则电子转移1 000 mol | |
| D. | 以上提取镁的过程涉及的离子反应共有3个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 主族元素都属于非金属元素 | |
| B. | 氧元素的相对原子质量为16 | |
| C. | 12C可用于测定古代出土文物的年代 | |
| D. | 氯气通入KI-淀粉溶液中会变蓝 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com