
【题目】要配制450mL 0.2molL﹣1FeSO4溶液,实验操作步骤有:
①在天平上称取a g绿矾(FeSO47H2O),将它放在烧杯中,用适量蒸馏水使其完全溶解;
②将所得溶液沿玻璃棒注入容量瓶中;
③继续向容量瓶中加水至液面距刻度线1﹣2cm处,改用胶头滴管滴加蒸馏水至凹液面底部与刻度线相切;
④用少量水洗涤烧杯和玻璃棒2﹣3次,每次洗液都转入容量瓶;
⑤将容量瓶塞紧,充分摇匀.
填写下列空白:
①a g绿矾的实际质量为 g.
②上述操作步骤的正确顺序为 .
③下列操作会使所配溶液的浓度偏高的是 .
A.若配制时遗漏步骤④; |
B.定容时俯视刻度线; |
C.称量时物、码放反了; |
D.绿矾样品已部分风化; |
E.摇匀后溶液低于刻度线,再加入蒸馏水使液面最低点与刻度线相切;
F.引流时玻璃棒靠在刻度线上方.
【答案】(1)27.8;
(2)①②④③⑤;
(3)BD.
【解析】试题分析:(1)要配制450mL 0.2molL﹣1FeSO4溶液,应选择500mL容量瓶,实际配制500mL溶液,依据m=CVM计算需要绿矾的质量;
(2)依据配制一定物质的量浓度溶液的一般步骤排序;
(3)分析操作对溶质的物质的量和溶液的体积的影响,依据C=![]() 进行误差分析.
进行误差分析.
解:(1)要配制450mL 0.2molL﹣1FeSO4溶液,应选择500mL容量瓶,实际配制500mL溶液,需要溶质的质量m=0.2mol/L×0.5L×278g/mol=27.8g;
故答案为:27.8;
(2)配制一定物质的量浓度溶液的一般步骤:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶,所以正确的操作为:①②④③⑤;
故答案为:①②④③⑤;
(3)A.若配制时遗漏步骤④,导致溶质的物质的量偏小,溶液浓度偏低,故A不选;
B.定容时俯视刻度线,导致溶液体积偏小,溶液浓度偏高,故B选;
C.依据左盘质量=右盘质量+游码质量,所以称量时物、码放反了,实际称量的固体为27﹣0.8=26.2g,溶质的物质的量偏小,溶液浓度偏低,故C不选;
D.绿矾样品已部分风化,27.8g固体中含有的溶质的物质的量偏大,溶液浓度偏高,故D选;
E.摇匀后溶液低于刻度线,再加入蒸馏水使液面最低点与刻度线相切,导致溶液体积偏大,溶液浓度偏低,故E不选;
F.玻璃棒在刻度线上方引流水,则易造成刻度线上方水有粘留,故定容完成后溶液体积会偏大,浓度会偏小,故F不选;
故选:BD.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】对于可逆反应:2SO2(g)+O2(g)![]() 2SO3(g),下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是( )
2SO3(g),下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是( )
A. 增大压强 B. 升高温度 C. 使用催化剂 D. 多充O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阅读、分析下列两个材料:
材料一
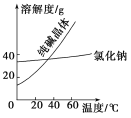
材料二
物质 | 熔点/℃ | 沸点/℃ | 密度/ g/cm3 | 溶解性 |
乙二醇(C2H6O2) | -11.5 | 198 | 1.11 | 易溶于水和乙醇 |
丙三醇(C3H8O3) | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互溶 |
常见的分离方法有以下几种:
A.蒸馏法
B.萃取法
C.“溶解、过滤、结晶”的方法
D.分液法
根据上述材料,回答下列问题(填序号):
(1)将纯碱从氯化钠和纯碱的混合物中分离出来,最好应用________;
(2)将乙二醇和丙三醇相互分离的最佳方法是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷中混有乙烯,欲除乙烯得到纯净的甲烷,可依次将其通过下列哪组试剂的洗气瓶( )
A.澄清石灰水,浓H2SO4
B.溴水,浓H2SO4
C.酸性高锰酸钾溶液,浓H2SO4
D.浓H2SO4,酸性高锰酸钾溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】饮食是保证我们身体健康的基本需求,下列关于饮食的说法正确的是( )
A.鸡蛋含有丰富的蛋白质,人类需要的蛋白质都可以由鸡蛋提供,多吃有益
B.水果、蔬菜含有丰富的维生素,有人为了减肥,每天只吃水果蔬菜即可
C.要促进身体健康,各种饮食必须合理搭配
D.米饭含有大量的淀粉,成人每天食用量不能超过200 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有甲、乙、丙、丁、戊五种短周期元素,原子序数依次增大,其常见化合价依次为+1、-2、+1、+3、-1。它们形成的物质间的转化关系如下图所示。常温下用惰性电极电解(有阳离子交换膜)1L l mol/L的A溶液。

请按要求回答下列问题:
(1)己元素与丙元素同主族,比丙原子多2个电子层,则己的原予序数为_____________;推测相同条件下丙、己单质分别与水反应剧烈程度的依据是____________________。
(2)甲、乙、戊按原予个数比1:1:1形成的化合物Y具有漂白性,其电子式为___________。
(3)上图转化关系中不属于氧化还原反应的有(填编号)____________。
(4)接通右图电路片刻后,向烧杯中滴加一种试剂即可检验铁电极被腐蚀,此反应的离子方程式为______。

(5)当反应①电解一段时间后测得D溶液pH=12(常温下,假设气体完全逸出,取出交换膜后溶液充分混匀,忽略溶液体积变化),此时共转移电子数目约为________;反应②的离子方程式为_______________。
(6)若上图中各步反应均为恰好完全转化,则混合物X中含有的物质(陈水外)有_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列应用不涉及氧化还原反应的是( )
A.Na2O2用作呼吸面具的供氧剂 B.工业上电解熔融状态的Al2O3制备Al
C.工业上利用合成氨实现人工固氮 D.实验室用NH4Cl和Ca(OH)2制备NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)3.6 g H2O的物质的量是________,含有____________________________个水分子,含有________mol H。
(2)11.7 g NaCl的物质的量是________,含有____________个Na+,________________个
Cl-,共含离子________mol。
(3)3.01×1022个OH-的物质的量为________,质量为________,含有质子的物质的量为________,含有电子的物质的量为________,这些OH-与________mol NH3的质量相同,和________g Na+含有的离子数相同。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com