
将一定量的有机物充分燃烧后的全部产物通入足量石灰水中,完全被吸收,经过滤得到沉淀20g,滤液质量比原石灰水减少5.8g,该有机物可能是( )
A、乙烯 B、甘油 C、乙醇 D、甲酸 甲酯
 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:
能源短缺是人类面临的重大问题。甲醇是一种可再生能源.具有广泛的开发和应用前景。因此甲醇被称为21世纪的新型燃料。
(1)工业上一般采用下列两种反应合成甲醇:
反应A:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1
CH3OH(g)+H2O(g) △H1
反应B:CO(g)+2H2(g)
 CH3OH(g) △H2
CH3OH(g) △H2
①下列条 件中,能说明反应A达到平衡状态的是 (2分)。
件中,能说明反应A达到平衡状态的是 (2分)。
A.生成甲醇的速率与生成水的速率相等
B.v(H2)/3=v(CH3OH)
C.恒容容器中,体系的压强不再改变
D.恒容容器中,混合气体密度不再发生改变
②在一定的压强下,将CO与H2的混合气体在催化剂作用下能自发反应生 成甲醇,则
成甲醇,则
△H2 0,△S 0(填“>”、“=”或“<”)(每空1分)。
③对于反应B,若容器容积不变,下列措施可增加甲醇产率的是 (2分)。
A.升高温度
B.将CH。OH(g)从体系中分离
C.充入He,使体系总压强增大
D.按原比例再充入CO和H。
④某温度下,将2mol CO和6mol H2,充人2L的密闭容器中,充分反应,达到平衡后,测得c(CO) =0.2 mol·L—1,则CO的转化率为 (2分),则该温度下该反应的平衡常数为 (2分)。
(2)已知在常温常压下:
①2CH3OH(I)十3O2(g) CO2(g)+4H2O(g) △H:-1275.6 kJ·mol—1
②2CO(g)+O2 (g)===2CO2 (g) △H= -566.0 kJ·mol—1
③H2O(g)===H2O(I) △H=- 44.0 kJ.mol-1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式 (2分).
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
A、淀粉和纤维素的通式都是(C6H10O5)n,是同分异构体
B、油脂属于酯类
C、油脂的氢化又叫油脂的硬化
D、葡萄糖能发生银镜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
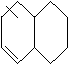
天然维生素P存在于槐树花蕾中,它是一种营养增补剂,关于维生素P的叙述中错误的是( )
 | |||||||
|
| ||||||
 | |||||||



|
|
 | |||
 | |||
(维生素P的结构简式)
A、可与溴水反应,且1mol物质与足量溴水反应消耗6mol Br2
B、可与NaOH溶液反应,1mol该物质可与4mol NaOH反应
C、一定条件下1mol该物质可与H2加成,耗H2最大量为7mol
D、维生素P遇FeCI3溶液发生显色反应
查看答案和解析>>
科目:高中化学 来源: 题型:
据报道,目前我国结核病的发病率有抬头的趋势,抑制结核杆菌的药物除雷米封外, (对氨基水杨酸钠)也是其中一种,它与雷米封同时服用,可以产生协同作用。
(对氨基水杨酸钠)也是其中一种,它与雷米封同时服用,可以产生协同作用。

|
|

 已知:
已知: ①
| |||
 | |||
②
 |
③
 |
④
PAS-Na(对氨基水杨酸钠)的合成路线如下:

|
| |||||||
 | |||||||
 | |||||||
| |||||||
|
 则:<1> 的化学方程式:_________________________;
则:<1> 的化学方程式:_________________________;
<2> C、D的结构式:C _________________,
D___________________;
<3> 指出反应类型 I:______________,II:_____________,
III:_________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中,属于水解反应且使溶液显酸性的是
A.CH3COOH+OH- CH3COO-+H2O
CH3COO-+H2O
B.HCO3—+ H2O  CO32- + H3O+
CO32- + H3O+
C.S2- + H2O HS-+ OH-
HS-+ OH-
D.NH4+ + H2O  NH3·H2O + H+
NH3·H2O + H+
查看答案和解析>>
科目:高中化学 来源: 题型:
在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:
 CO(g) +H2O(g)
CO(g) +H2O(g)  CO2(g) +H2 (g) △H<0。
CO2(g) +H2 (g) △H<0。
(1)CO和H2O浓度变化如右图,则在该温度下,该反应
的平衡常数K= 。
0~4min的平均反应速率v(CO)=_____mol·L-1·min-1。若降低温度,该反应的K值将 ,该反应的化学反应速率将 (填“增大”“减小”或“不变”)。
(2)在相同容器中发生上述反应,当温度高于850℃时,
容器内各物质的浓度变化如下表。
| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
①表中3min~4min之间反应处于_________状态; c 1数值_________0.08 mol·L-1 (填大于、小于或等于)。
②反应在4min~5min间,平衡向逆方向移动,可能的原因是_________
a.增加水蒸气 b.降低温度
c.使用催化剂 d.增加氢气浓度
(3)在相同温度下(850℃),若起始时c(CO)=1mol·L-1,c(H2O)=2mol·L-1,反应进行一段时间后,测得H2的浓度为0.5 mol·L-1,则此时该反应是否达到平衡状态 (填“是”与“否”),此时v(正) v(逆)(填“大于”“小于”或“等于”),你判断的依据是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,水的离子积约为10-12,将Va L pH=2的硫酸溶液与Vb L pH=11的NaOH溶液混合,若混合溶液的pH=10,体积是(Va+Vb) L,则Va∶Vb为
A.2∶11 B.11∶2 C.9∶2 D.2∶9
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com