
| A、分子数目:①=②=③ |
| B、质量关系:①<③<② |
| C、压强关系:①>③>② |
| D、原子数目:②>③>① |
| m |
| M |
| m |
| M |


 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:
| c(OH-) |
| c(NH3?H2O) |
| A、①②③ | B、①③⑤ |
| C、①③⑥ | D、②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| T/K | T1 | T2 | T3 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、O原子的电子排布图为 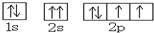 |
| B、氯化钠的分子式:NaCl |
C、Cl-的结构示意图: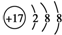 |
| D、Ca原子的电子排布式为 1s22s22p63s23p63d2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧化性:F2>C12>Br2 |
| B、酸性:HClO4>H2SO4>H3PO4 |
| C、碱性:NaOH>Mg(OH)2>Al(OH)3 |
| D、热稳定性:SiH4>PH3>H2S |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,23g NO2含有NA个氧原子 |
| B、标准状况下,22.4L H2O含有NA个H2O分子 |
| C、含10 NA个电子的N2分子的物质的量是1mol |
| D、0.1mol/L的Ba(OH)2溶液中,OH-的个数为0.2NA个 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、稀硫酸与铁粉反应:2Fe+6H+=2Fe3++3H2↑ |
| B、氯化铜溶液与铁粉反应:Cu2++Fe=Fe2++Cu |
| C、碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑ |
| D、氢氧化钡溶液与稀硫酸反应:Ba2++SO42-=BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用盐酸清除水垢CaCO3+2H+=Ca2++CO2↑+H2O |
| B、Fe跟稀硫酸反应:Fe+2H+=Fe2++H2↑ |
| C、澄清石灰水跟稀盐酸:H++OH-=H2O |
| D、碳酸氢钠溶液跟氢氧化钠溶液反应 HCO3-+OH-=H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
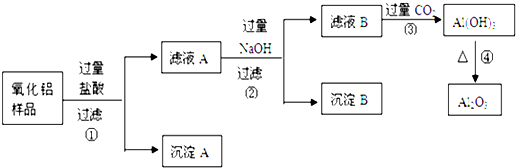
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com