
【题目】(1)目前常用的镍(Ni)镉(Cd)电池,其电池总反应可表示为:Cd+2NiO(OH)十2H2O![]() 2 Ni(OH)2+ Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难于溶水但能溶于酸。正极的反应式是____________________,负极的反应式是_________________。
2 Ni(OH)2+ Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难于溶水但能溶于酸。正极的反应式是____________________,负极的反应式是_________________。
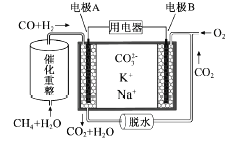
(2)一种熔融碳酸盐燃料电池原理示意如图: 电池工作时,外电路上电流的方向应从电极___(“填A或B”)流向用电器。内电路中,CO32-向电极_____(“填A或B”)移动,电极A上CO参与的电极反应为______________________。
(3)将两铂片插入KOH溶液中作为电极,在两极区分别通入甲烷和氧气构成燃料电池,则通入甲烷气体的电极是原电池的____极,该极的电极反应式是____________________,电池工作时的总反应的离子方程式是__________________。如果消耗甲烷160g,假设化学能完全转化为电能,则转移电子的数目为___________(用NA表示),需要消耗标准状况下氧气的体积为_______L。
【答案】 2NiO(OH)+2e-+2H2O=2Ni(OH)2+2OH- Cd-2e-+2OH-=Cd(OH)2 B A CO-2e-+CO32-=2CO2 负 CH4+10OH――8e-=CO32-+7H2O CH4+2O2+2OH-=CO32-+3H2O 80NA 448
【解析】(1)由电池的总反应可知,该电池放电时,镉在负极上被氧化生成氢氧化镉、氢氧化氧镍在正极上被还原生成氢氧化镍,故正极的反应式是2NiO(OH)+2e-+2H2O=2Ni(OH)2+2OH-,负极的反应式是Cd-2e-+2OH-=Cd(OH)2。
(2)由该燃料电池原理示意图可知,燃料由电极A通入、氧气和二氧化碳由电极B通入,则A为负极、B为正极,所以,电池工作时,外电路上电流的方向应从电极B流向用电器。内电路中,CO32-向电极负极A移动,电极A上CO参与的电极反应为CO-2e-+CO32-=2CO2。
(3)将两铂片插入KOH溶液中作为电极,在两极区分别通入甲烷和氧气构成燃料电池,则通入甲烷气体的电极是原电池的负极,该极的电极反应式是CH4+10OH――8e-=CO32-+7H2O,电池工作时的总反应的离子方程式是CH4+2O2+2OH-=CO32-+3H2O。160g甲烷的物质的量为10mol,根据负极的电极反应式可知,消耗10mol 甲烷要转移80mol电子,则转移电子的数目为80NA,需要消耗氧气的物质的量为80mol![]() 20mol,这些氧气在标准状况下的体积为20mol
20mol,这些氧气在标准状况下的体积为20mol![]() 22.4L/mol=448L。
22.4L/mol=448L。


科目:高中化学 来源: 题型:
【题目】X,Y,Z均为中学化学常见物质,在一定条件下,X能与强酸或强碱溶液发生如图的反应(部分反应物、生成物及反应条件略去).则下列说法不正确的是( ) ![]()
A.若X为金属单质,则Y、Z可能为同一物质
B.若X为盐,则Y一定是CO2
C.若X为盐,则Z一定能使湿润的红色石蕊试纸变蓝
D.若X为盐,则其水溶液中水的电离程度比同温度下纯水的电离程度大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸的年产量可以用来衡量一个国家的化工生产能力.工业生产硫酸的流程中存在反应:2SO2(g)+O2(g)2SO3(g).反应体系中SO3的百分含量和温度的关系如图所示(曲线上任何一点都表示平衡状态).根据图示回答下列问题:
(1)画出硫原子的结构示意图
(2)下列说法正确的是a.若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡不移动
b.在D点时,v正>v逆
c.B点、C点反应的平衡常数分别为K1、K2 , 则K1<K2
d.在A点时,消耗1mol SO2必定同时消耗1mol SO3 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于苯乙烯的下列叙述中,正确的是( ) ①能使酸性KMnO4溶液褪色;
②可发生加成反应;
③可溶于水;
④可溶于苯中;
⑤能与浓硝酸在浓H2SO4作用下发生取代反应;
⑥所有的原子可能共平面.
A.①②③④⑤
B.①②⑤⑥
C.①②④⑤⑥
D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系:甲 ![]() 乙
乙 ![]() 丙.下列有关物质的推断不正确的是( )
丙.下列有关物质的推断不正确的是( )
A.若甲为焦炭,则丁可能是O2
B.若甲为SO2 , 则丁可能是氨水
C.若甲为Fe,则丁可能是盐酸
D.若甲为NaOH 溶液,则丁可能是CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含有NaBr和KI的混合溶液中通入过量的Cl2充分反应,将溶液蒸干,并灼烧所得的物质,最后剩余的固体是
A.NaCl 和 KIB.KCl 和 NaCl
C.NaCl 和 NaBrD.NaCl、KCl 和 Fe
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,两个等体积的干燥圆底烧瓶中分别充满①NH3,②NO2,进行喷泉实验,经充分反应后,瓶内溶液的物质的量浓度为
A.①=②B.①>②C.①<②D.不能确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com