
����Ŀ���£�N2H4���������ķ�Ӧ������¶�Ӱ�졣ijͬѧ��Ʒ���̽���¶ȶԲ���Ӱ��Ľ����ͼ��ʾ������˵������ȷ����
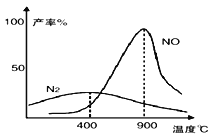
A. �¶Ƚϵ�ʱ�� �º�������Ҫ�����ķ�ӦN2H4��O2 = N2��2H2O
B. 900��ʱ���ܷ��� N2��O2 = 2NO
C. 900��ʱ�� N2�IJ����� NO �IJ���֮�Ϳ���С�� 1
D. ��̽�������ǽ�һ�������º����������ܱ������н��в�������ʵ��
���𰸡�D
��������A. ��ͼ��֪���¶Ƚϵ�ʱ���º�������Ҫ�����ķ�ӦN2H4��O2 = N2��2H2O��A��ȷ��B. ��ͼ��֪����400�浽900��֮�䣬N2�IJ�����С�� NO �IJ��������ߣ����ԣ�900��ʱ���ܷ��� N2��O2 = 2NO��B��ȷ��C. ��ͼ��֪�����¶ȸ���900���N2�IJ����� NO �IJ��ʶ������ˣ�˵��������Ӧ���ǿ��淴Ӧ������900��ʱ�� N2�IJ����� NO �IJ���֮�Ϳ���С��1��C��ȷ��D. ��̽�������ǽ�һ�������º����������ܱ����������ڲ�ͬ�¶��´ﵽƽ���ʵ������Ӧ�ﵽƽ����Ҫһ����ʱ�䣬���Բ��ܲ��������¶ȣ�D����ȷ������ѡD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ƭ�����������ð֢״����ṹ��ʽ��ͼ�������й�˵���������

A. ����ҵķ���ʽΪC13H18O2 B. ������뱽������ͬϵ��
C. 1mol������������3mol���������ӳɷ�Ӧ D. ������ڱ����Ϸ���ȡ����Ӧ����һ�ȴ�����4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݲ�ͬ�ķ������HNO3�����������е���һ��
�������� �ں����� ��һԪ�� �ܻ���� �ݵ����
A. �ڢۢ� B. �٢ڢ� C. �٢ڢ� D. �ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NH4HSO4 �ڷ����Լ���ҽҩ�����ӹ�ҵ����;�㷺������ʱ����100mL0.lmol��L-1 NH4HSO4 ��Һ�еμ�0.1mol��L-1NaOH��Һ���õ�����ҺpH ��NaOH ��Һ����Ĺ�ϵ������ͼ��ʾ������˵����ȷ����
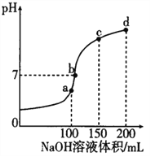
A. a����Һ�У�c(NH4+)+c(H+)=c(Na+) +c(OH-)
B. c����Һ�У�c(SO42-)>c(NH3��H2O)>c(NH4+)
C. d����Һ�У�c(SO42-) >c(NH4+)>c(OH-)
D. a��b��c��d �ĸ����У�b��ˮ�ĵ���̶����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ˮ�ĵ���ƽ����������ͼ��ʾ������˵����ȷ���ǣ� ��
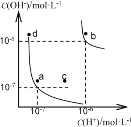
A. ͼ�ж�Ӧ����¶ȹ�ϵΪ�� a��b
B. ˮ�ĵ��볣��KW��С��ϵΪ��b��d
C. �¶Ȳ��䣬��������NaOH��ʹ��Һ��c��䵽a��
D. b���Ӧ�¶��£���pH=2��H2SO4��pH=10��NaOH��Һ�������Ϻ���Һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼI��ʾ���ס���֮��ĸ���K�ͻ���F�����������ƶ���F��ѹ���㶨�����г���2mol A��1mol B�����г���2mol C��1mol He����ʱKͣ��0������һ�������·������淴Ӧ��2A(g��+B(g��![]() 2C(g������Ӧ�ﵽƽ����ٻָ���ԭ�¶ȣ�������˵����ȷ���ǣ� ��
2C(g������Ӧ�ﵽƽ����ٻָ���ԭ�¶ȣ�������˵����ȷ���ǣ� ��

A. �ﵽƽ��ʱ����K����ͣ����0�̶�����2��4֮��
B. ���ﵽƽ��ʱ����K����ͣ�������1����������C��ת����С��50%
C. ��ͼII��ʾ��x���ʾʱ�䣬��y��ɱ�ʾ�ס���������������������ʵ�����A�����ʵ���
D. ���ﵽƽ��ʱ����K����ͣ��������2����������F����ͣ�����Ҳ�̶ȴ���4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��50g̼��������ȼ�գ��õ��������CO��CO2����֪C(s)+1/2O2(g)��CO(g)��H=��110.35kJ/mol��CO(g)+1/2O2(g) ��CO2(g)��H=��282.57kJ/mol�� ����ȫȼ�������ʧ��������ʵ�ʷų�������֮�ȴ�Լ��( )
A. 55:141 B. 283:503 C. 1:1 D. 141:196
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����3�������Ϊ1 L�ĺ����ܱ������з�����Ӧ��SO2(g)��2NO(g)![]() 2NO2(g)��S(s)���ı�����I�ķ�Ӧ�¶���ƽ��ʱc( NO2)���¶ȵĹ�ϵ����ͼ��ʾ������˵����ȷ����
2NO2(g)��S(s)���ı�����I�ķ�Ӧ�¶���ƽ��ʱc( NO2)���¶ȵĹ�ϵ����ͼ��ʾ������˵����ȷ����
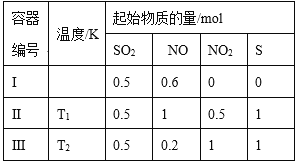
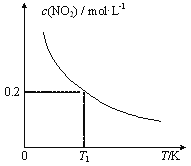
A. �÷�Ӧ����H<0
B. T1ʱ���÷�Ӧ��ƽ�ⳣ��Ϊ![]()
C. ������������������T1ʱ�ﵽƽ�⣬��ѹǿ֮��С��1:2
D. ��T2<T1���ﵽƽ��ʱ����������NO���������С��40%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪Am+��Bn-������ͬ�ĺ�������Ų�����Aԭ�ӵ�������ΪX����Bԭ�ӵ�������Ϊ�� ��
A.X-m-nB.X+m+nC.X+m-nD.X-m+n
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com