
为了提高煤的利用率,人们先把煤转化为CO和H2,再将它们转化为甲醇,某实验人员在一定温度下的密闭容器中,充入一定量的H2和CO,发生反应:2H2(g)+CO(g) CH3OH(g),测定的部分实验数据如下:
CH3OH(g),测定的部分实验数据如下:
t/s 0 500 1 000
c(H2)/(mol•L﹣1) 5.00 3.52 2.48
c (CO)/(mol•L﹣1) 2.50
1.76
1.24
(1)在500s内用H2表示的化学反应速率是
(2)在1 000s内用CO表示的化学反应速率是,1 000s时CO的转化率是50.4%.
(3)在500s时生成的甲醇的浓度是.
考点: 化学平衡的调控作用.
专题: 化学平衡专题.
分析: 据化学方程式求算500s和1000s时CO的浓度;
(1)根据表中数据及v=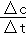 计算出在500s内用H2表示的化学反应速率;
计算出在500s内用H2表示的化学反应速率;
(2)根据反应速率表达式v=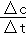 计算出1000s内用氢气表示的化学反应速率,然后根据化学计量数与反应速率成正比计算出氢气的反应速率;根据反应速率计算出氢气的转化率;
计算出1000s内用氢气表示的化学反应速率,然后根据化学计量数与反应速率成正比计算出氢气的反应速率;根据反应速率计算出氢气的转化率;
(3)根据氢气的反应速率计算出消耗氢气的物质的量,再计算出在500s时生成的甲醇的浓度.
解答: 解:据化学方程式中的化学计量数之比等于反应速率之比,求算出CO在500s时的浓度为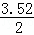 =1.76,1000s时的浓度为
=1.76,1000s时的浓度为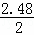 =1.24,故答案为:1.76;1.24;
=1.24,故答案为:1.76;1.24;
(1)在500s内用H2表示的化学反应速率为:v(H2)=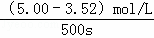 =2.96×10﹣3mol/(L•s),故答案为:2.96×10﹣3mol/(L•s);
=2.96×10﹣3mol/(L•s),故答案为:2.96×10﹣3mol/(L•s);
(2)在1000s内用氢气表示的化学反应速率是:v(H2)= =2.52×10﹣3mol/(L•s),则1000s内用CO表示的化学反应速率为:v(CO)=
=2.52×10﹣3mol/(L•s),则1000s内用CO表示的化学反应速率为:v(CO)=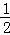 v(H2)=1.26×10﹣3mol/(L•s);1000s时H2的消耗浓度为:△c(H2)=(5.00﹣2.48)mol/L=2.52mol/L,氢气的转化率为
v(H2)=1.26×10﹣3mol/(L•s);1000s时H2的消耗浓度为:△c(H2)=(5.00﹣2.48)mol/L=2.52mol/L,氢气的转化率为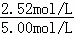 ×100%=50.4%,
×100%=50.4%,
故答案为:1.26×10﹣3mol/(L•s);50.4%;
(3)在500s时氢气的浓度变化为:△c(H2)=(5.00﹣3.52)mol/L=1.48mol/L,由反应2H2(g)+CO(g)⇌CH3OH(g)可知,生成甲醇的物质的量浓度为:c(CH3OH)=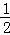 △c(H2)=0.74mol/L,故答案为:0.74mol/L.
△c(H2)=0.74mol/L,故答案为:0.74mol/L.
点评: 本题考查了反应速率的计算,题目难度中等,注意明确化学反应速率与化学计量数成正比,掌握化学反应速率的概念及其表达式.


科目:高中化学 来源:2014-2015学年浙江省金华十校高三下学期高考模拟(4月)理综化学试卷(解析版) 题型:实验题
二草酸合铜(Ⅱ)酸钾晶体{K2[Cu(C2O4)2]·2H2O}制备流程如下:

(已知:H2C2O4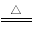 CO↑+CO2↑+H2O)
CO↑+CO2↑+H2O)
(1)制备CuO:CuSO4溶液中滴入NaOH溶液,加热煮沸、冷却、双层滤纸过滤、洗涤。
①用双层滤纸过滤的原因是 。
②用蒸馏水洗涤氧化铜时,如何证明氧化铜已洗涤干净 。
(2)为了提高CuO的利用率,如何让CuO充分转移到热的KHC2O4溶液中 ;50℃水浴加热至反应充分,发生反应的化学方程式为 ;再经趁热过滤、沸水洗涤、将滤液蒸发浓缩得到二草酸合铜(Ⅱ)酸钾晶体。
(3)本实验用K2CO3粉末与草酸溶液反应制备KHC2O4,而不用KOH粉末代替K2CO3粉末,其主要原因是 。
(4)二草酸合铜(Ⅱ)酸钾晶体的制备也可以用CuSO4晶体和K2C2O4溶液反应得到。从硫酸铜溶液中获得硫酸铜晶体的实验步骤为:加入适量乙醇、蒸发浓缩、冷却结晶、过滤、洗涤、干燥。①加入适量乙醇的优点有:
a.缩短加热的时间,降低能耗;
b. 。
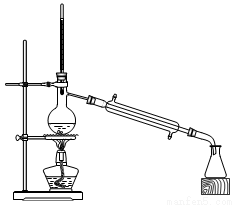
②在蒸发浓缩的初始阶段还采用了如图所示的装置,其目的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X(g)+3Y(g)⇌2Z(g)的△H<0,在恒容密闭容器中反应达到平衡时,下列说法正确的是( )
|
| A. | 升高温度,平衡将正向移动 |
|
| B. | 3V正(X)═V逆(Y) |
|
| C. | 降低温度,混合气体的密度变小 |
|
| D. | 增加X的物质的量,Y的转化率降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于化学反应速率的说法,不正确的是()
A. 化学反应速率是衡量化学反应进行快慢程度的物理量
B. 化学反应速率的大小主要取决于反应物的性质
C. 化学反应速率常用单位时间内生成某物质的质量的多少来表示
D. 化学反应速率常用单位有:mol•L﹣1•s﹣1和mol•L﹣1•min﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:①2C(s)+O2(g)═2CO(g)△H=﹣221.0kJ•mol﹣1;
②2H2(g)+O2(g)═2H2O(g)△H=﹣483.6kJ•mol﹣1.
则制备水煤气的反应C(s)+H2O(g)═CO(g)+H2(g)的△H为()
A. 262.6 kJ•mol﹣1 B. ﹣131.3 kJ•mol﹣1
C. ﹣352.3 kJ•mol﹣1 D. 131.3 kJ•mol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列装置所示的实验中,能达到实验目的的是( )
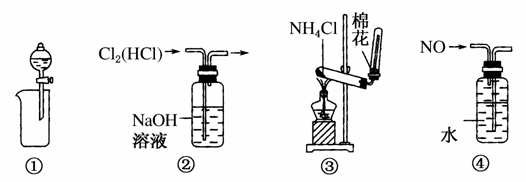
A.①从Mg(OH)2悬浊液中分离出Mg(OH)2
B.②除去Cl2中的HCl
C.③实验室制氨气
D.④排水法收集NO
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示装置中,M棒变细,N棒变粗.由此判断下表中所列M、N、R物质,其中合理的是()
M N R
A 锌 铜 稀硫酸
B 铜 铁 稀盐酸
C 铁 铜 硝酸银
D 铜 铁 氯化铁
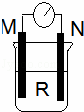
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
某元素原子最外层上只有两个电子,该元素()
A. 一定是金属元素
B. 一定是ⅡA族元素
C. 一定是过渡元素
D. 可能是金属元素,也可能不是金属元素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com