
【题目】将物质的量相等的硫酸铝和硫酸铵溶于水形成VmL混合溶液,向混合溶液中逐滴加入某氢氧化钠溶液(其物质的量浓度为混合溶液中两溶质的物质的量浓度之和),直至过量.下列表示氢氧化钠溶液加入的体积(x)与溶液中沉淀物的量(y)的关系示意图中正确的是( )
A. 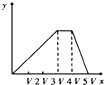 B.
B. 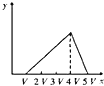
C. 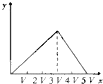 D.
D. 
【答案】A
【解析】假定含有Al2(SO4)3 ,(NH4)2 SO4的物质的量分别为1mol,反应顺序 :开始滴加NaOH发生为Al3++3OH-=Al(OH)3 ↓,沉淀逐渐增大,当Al3+沉淀完全时需加入6molOH-,生成Al(OH)3 2mol,达最大值;再发生NH4++OH-=NH3·H2O;NH4+完全反应时需2molOH-,该过程中沉淀氢氧化铝的量不变;最后继续加NaOH,发生反应Al(OH)3 +OH-=AlO2-+2H2O,直到2molAl(OH)3 溶解,需再加入2molNaOH。三段过程消耗NaOH的物质的量之比为6mol:2mol:2mol=3:1:1,三阶段消耗NaOH溶液的体积比为3:1:1。
A、从图象可知,开始滴加NaOH,即生成沉淀,达最大后,(铝离子完全反应)继续加NaOH,铵根离子开始反应,沉淀不变,当铵根离子反应完毕,氢氧根使氢氧化铝沉淀溶解,至最后消失,三阶段消耗NaOH溶液的体积比为3:1:1,图象A符合,故A正确;B、图为先与铵根离子反应,离子反应的顺序错误,故B错误;C、未考虑铵根离子的反应、氢氧化铝溶解消耗的氢氧化钠的物质的量不相符,故C错误;D、三阶段消耗NaOH溶液的体积比为3:1:1,图中比例为2:1:3不符合,故D错误。故选。


科目:高中化学 来源: 题型:
【题目】某兴趣小组用下图所示装置制备气体(酒精灯可以根据需要选择),对应说法正确的是

选项 | ①中药品 | ②中药品 | ③中药品 | ④中药品 | 制备气体 | ⑥中药品及作用 |
A | 浓盐酸 | MnO2 | 饱和食盐水 | 浓硫酸 | C12 | NaOH溶液,尾气吸收 |
B | 稀硝酸 | Cu | 烧碱溶液 | 浓硫酸 | NO | Na()H溶液,尾气吸收 |
C | 浓盐酸 | 大理石 | 饱和Na2CO3溶液 | 浓硫酸 | CO2 | 澄清石灰水,检验CO2 |
D | 浓盐酸 | Zn | 水 | 浓硫酸 | H2 | 可撤去 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将下列各组物质, 分别按等物质的量混合后加水溶解, 有沉淀生成的是( )
A. AlCl3、Ba(OH)2、HNO3B. CaCl2、NaHCO3、HCl
C. Na2CO3、NaAlO2、NaOHD. AlCl3、K2SO4、HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100mL该溶液进行如下实验:(已知:NH4++OH-![]() NH3↑+H2O)
NH3↑+H2O)
(1)第一份加入AgNO3溶液有沉淀产生;
(2)第二份加足量NaOH溶液加热后,收集到0.08mol气体;
(3)第三份加足量BaCl2溶液后,得干燥沉淀12.54g,经足量盐酸洗涤干燥后,沉淀质量为4.66g。根据上述实验,回答以下问题。
(1)由第一份进行的实验推断该混合物是否一定含有Cl-?________(答是或否)
(2)由第二份进行的实验得知混合物中应含有_____(填离子符号),其物质的量浓度为______。
(3)由第三份进行的实验可知12.54g沉淀的成分为________。
(4)综合上述实验,你认为以下结论正确的是_________。
A.该混合液中一定有K+、NH4+、CO32-、SO42-,可能含Cl-,且n(K)≥0.04mol
B.该混合液中一定有NH4+、CO32-、SO42-,可能含有K+、Cl-
C.该混合液中一定有NH4+、CO32-、SO42-,可能含有Mg2+、K+、Cl-
D.该混合液中一定有NH4+、SO42-,可能含有Mg2+、K+、Cl-
(5)我国政府为消除碘缺乏病,规定在食盐中必须加入适量的碘酸钾。检验食盐中是否加碘,可利用如下反应:KIO3+KI+H2SO4=K2SO4+I2+H2O
①配平该方程式,并且用单线桥法表示该方程式电子转移的方向和数目:________。
②该反应中氧化剂和还原剂的物质的量之比为_____________。
③如果反应中转移0.5mol电子,则生成I2的物质的量为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氰[(CN)2]的化学性质与卤素(X2)很相似,化学上称之为拟卤素,其氧化性介于Br2和I2之间,下列有关反应方程式不正确的是
A. (CN)2和NaOH溶液反应:(CN)2+2OH-=CN-+CNO-+H2O
B. MnO2和HCN反应:MnO2+4HCN(浓)![]() Mn(CN)2+(CN)2↑+2H2O
Mn(CN)2+(CN)2↑+2H2O
C. 在NaBr和KCN混合溶液中通入少量Cl2:Cl2+2CN-=2Cl-+(CN)2
D. 向KCN溶液中加入碘水:I2+2KCN=2KI+(CN)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是常见的电化学装置图,①③④中均为惰性电极,下列说法不正确的是

A. 装置①中正极反应式为:2Cl--2e-=Cl2,负极反应式为:Cu2++2e-=Cu
B. 装置②中铜片为阳极,若铜片和铁制品的质量相等,电解一段时间后,电路中有2mol电子转移,此时此时铜片和铁制品的质量差128g
C. 装置③中b极为正极,该极的电极反应方程式为O2+2H2O+4e-=4OH-
D. 装置④阴极的纯水中加入NaOH的作用是:增大离子浓度,增强溶液的导电性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.对同类事物进行再分类可用树状分类法
B.对某物质的分类不可能有多个标准
C.试管、烧杯和容量瓶都可以直接用来加热
D.分液是提纯或分离几种互溶且沸点不同的液体混合物的方法
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com