
下列叙述正确的是
A.一定温度、压强下,气体体积由其分子的大小决定
B.一定温度、压强下,气体体积由其物质的量的多少决定
C.气体摩尔体积是指1 mol任何气体所占的体积为22.4 L
D.不同的气体,若体积不等,则它们所含的分子数一定不等
科目:高中化学 来源: 题型:
类推的思维方法在化学学习与研究中有时会产生错误的结论,因此类推的结论最终要经过实践的检验才能确定其正确与否,下列几种类推结论中,错误的是( )
①钠与水反应生成NaOH和H2;所有金属与水反应都生成碱和H2。
②铁露置在空气中一段时间后就会生锈;性质更活泼的铝不能稳定存在于空气中。
③化合物NaCl的火焰颜色为黄色;Na2CO3的火焰颜色也为黄色。
④密度为1.1 g·cm-3与密度为1.2 g·cm-3的NaCl溶液等体积混合,所得NaCl溶液的密度介于1.1 g·cm -3与1.2 g·cm-3之间;Na—K合金的熔点应介于Na和K的熔点之间。
A.①② B.①④ C.①②③④ D.①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.在常温、常压下,11.2 L N2含有的分子数为0.5NA
B.标准状况下,22 .4 L H2和O2的混合物所含分子数为NA
.4 L H2和O2的混合物所含分子数为NA
C.标准状况下,18 g H2O的体积是22.4 L
D.1 mol SO2的体积是22.4 L
查看答案和解析>>
科目:高中化学 来源: 题型:
同温、同压下,甲、乙两容器分别盛有甲烷和氨气,已知它们所含原子数相同,则甲、乙两容器的体积比是( )
A.4∶3 B.5∶4 C.4∶5 D.1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
在相同的温度和压强下,4个容器中分别装有4种气体。已知各容器中的气体和容器的容积分别是a. CO2,100mL;b. O2,200mL;c.N2,400mL;d.CH4600mL。则4个容器中气体的质量由大到小的顺序是
A.a>b>c>d B.b>a>d>c C.c>d>b>a D.d>c>a>b
查看答案和解析>>
科目:高中化学 来源: 题型:
以下一些氧化物和单质之间可发生如图所示的反应:

其中,氧化物(Ⅰ)是红棕色固体、氧化物(Ⅱ)、(Ⅲ)、(Ⅳ)在反应条件下都是气体。
(1)氧化物(Ⅰ)的化学式(分子式)是________,氧化物(Ⅱ)的化学式(分子式)是________。
(2)反应①的化学方程式是________________ ,
反应②的化学方程式是________________,
反应③的化学方程式是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
过氧化钙可以用于改善地表水质,处理含重金属粒子废水和治理赤潮,也可用于应急供氧等。工业上生产过氧化钙的主要流程如下:
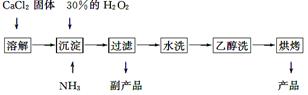
已知CaO2·8H2O呈白色,微溶于水,加热至350 ℃左右开始分解放出氧气。
(1)用上述方法制取CaO2·8H2O的化学方程式是______________________________;
(2)检验“水洗”是否合格的方法是___________________________________________;
(3)沉淀时常用冰水控制温度在0 ℃左右,其可能原因是______________________;
(4)测定产品中CaO2的含量的实验步骤:
第一步:准确称取a g产品于有塞锥形瓶中,加入适量蒸馏水和过量的b g KI晶体,再滴入少量2 mol·L-1的H2SO4溶液,充分反应。
第二步:向上述锥形瓶中加入几滴淀粉溶液。高 考 资 源 网
第三步:逐滴加入浓度为c mol·L-1的Na2S2O3溶液至反应完全,消耗Na2S2O3溶液V mL。
【已知:I2+2S2O32-=2I-+S4O62-】
①第一步发生的反应的化学方程式为 ;
CaO2的质量分数为____________(用字母表示);
②某同学第一步和第二步的操作都很规范,第三步滴速太慢,这样测得的CaO2的质量分数可能________(填“不受影响”、“偏低”或“偏高”),原因是___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com