
| A、25℃时,Mg(OH)2固体在氨水中的Ksp比在NH4Cl溶液中的Ksp小 |
| B、25℃时,向Mg(OH)2的澄清饱和溶液中加入少量NH4Cl固体,c(Mg2+)减小 |
| C、25℃时,Mg(OH)2的溶解能力大于MgF2的溶解能力 |
| D、25℃时,饱和Mg(OH)2溶液与0.1mol?L-1NaF溶液等体积混合,能生成MgF2沉淀 |


科目:高中化学 来源: 题型:
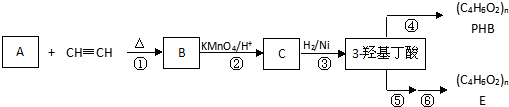
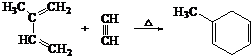

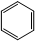
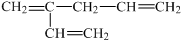

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 操作 | 现象 | 结论 |
| A | 将Cu片小心放入浓H2SO4中,加热 | 生成刺激性气味气体 | Cu与浓H2SO4反应生成SO2 |
| B | 向AgNO3溶液中滴加过量氨水 | 溶液澄清 | Ag+与NH3?H2O能大量共存 |
| C | 向某溶液滴加硝酸酸化的BaCl2溶液 | 有白色沉淀生成 | 该溶液中一定含有SO42- |
| D | 某无色溶液中滴加氯水和CCl4,振荡、静置 | 下层溶液显紫色 | 原溶液中有I- |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、热稳定性:Na2CO3>NaHCO3>H2CO3 |
| B、相同pH的溶液,加水稀释后的pH:H2SO4>HCl>CH3COOH |
| C、离子半径:K+>Na+>Mg2+ |
| D、结合H+能力:OH->ClO->NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、少量的金属钠长期暴露在空气中,它的最终产物是NaHCO3 |
| B、向紫色石蕊溶液中加入过量Na2O2粉末,振荡,产生气泡,溶液仍为紫色 |
| C、CO与H2混合气体3 g和足量的氧气燃烧后,在150℃时将混合气体通过足量的Na2O2后,Na2O2增重的质量为3g |
| D、将1g Na2CO3和NaHCO3分别溶于10mL水中,滴入酚酞试液后溶液所显红色深浅相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| /s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A、反应在前50 S内的平均速率v(PCl3)=0.0032mol/(L?s) |
| B、保持其他条件不变,升高温度,平衡时c(PCl3=0.11)mol?L-1,该反应为放热反应 |
| C、相同温度下,起始时向容器中充入1.0 mol PC15、0.20 mol PC13和0.20 mo1 C12,达到平衡的v(正)>v(逆) |
| D、相同温度下,起始时向容器中充入2.0 mol PC13、2.0 mol C12,达到平衡时,PCl3的转化率小于80% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com