
| A. | 水玻璃保存在用橡皮塞的玻璃试剂瓶中 | |
| B. | 氢氟酸保存在用橡皮塞的玻璃试剂瓶中 | |
| C. | 固体烧碱放在广口塑料瓶中并且塑料盖盖严 | |
| D. | 液溴密封盛放在棕色瓶中,液面放一层水 |
分析 A.水玻璃具有粘合性,不能使用玻璃塞;
B.氢氟酸与玻璃中的二氧化硅反应;
C.固体放在广口瓶中,且碱与二氧化硅反应;
D.溴易挥发,且溴水中HBrO光照分解.
解答 解:A.水玻璃具有粘合性,不能使用玻璃塞,则水玻璃保存在用橡皮塞的玻璃试剂瓶中,故A正确;
B.氢氟酸与玻璃中的二氧化硅反应,则氢氟酸保存在用橡皮塞的塑料试剂瓶中,故B错误;
C.固体放在广口瓶中,且碱与二氧化硅反应,则固体烧碱放在广口塑料瓶中并且塑料盖盖严,防止潮解,故C正确;
D.溴易挥发,且溴水中HBrO光照分解,则液溴密封盛放在棕色瓶中,液面放一层水,故D正确;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、发生的反应及化学试剂的保存为解答的关键,侧重分析与实验能力的考查,注意元素化合物与实验的结合,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 与H2化合的能力:At2>I2 | B. | 砹在常温下为白色固体 | ||
| C. | AgAt易溶于水 | D. | 砹难溶于水,易溶于四氯化碳 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ②③ | C. | ①③ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaF>NaCl>NaBr>Nal | B. | NaCl<MgC12<AlCl3>SiCl4 | ||
| C. | LiF>NaCl>KBr>Csl | D. | Al2O3>MgO>CaO>BaO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
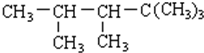
| A. | 2-乙基戊烷 | B. | 2,3-二甲基庚烯 | ||
| C. | 2,3-二甲基-5-庚烯 | D. | 2,2,3,4-四甲基戊烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学式符合Cn(H2O)m组成的一定是糖 | B. | 糖类物质都不能水解 | ||
| C. | 自然界中无单糖 | D. | 糖类物质是人类最基本的能量来源 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③④ | B. | ①③⑤ | C. | ①③④ | D. | ②⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
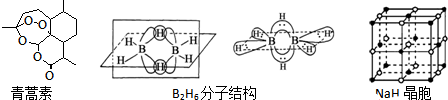
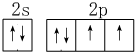 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 24gNaH中阴离子所含电子总数为NA | |
| B. | 标准状况下,22.4L苯中含有C-H键数目为6NA | |
| C. | CO2通过Na2O2使其增重a g时,反应中转移的电子数为aNA/28 | |
| D. | 常温常压下,14.9 g KCl与NaClO的固体混合物中阴离子的数目为0.15 NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com