
已知元素X、Y、Z、W、R为前四周期元素,且原子序数依次增大。X基态原子核外有三个未成对电子,Z、W分别是短周期中电负性最大和最小的元素;R2+离子的3d轨道中有三对成对电子。请回答下列问题:
(1)R基态原子的电子排布式为 ,元素X、Y、Z的第一电离能由大到小的顺序为(用元素符号表示) 。
(2)化合物XZ3的空间构型为 ,R2+与NH3形成的配离子中,提供孤对电子的是 。
(3)Z的氢化物由固体变为气态所需克服的微粒间的作用力是 。
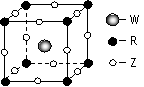 (4)Z、W、R形成某种化合物的晶胞结构如右图所示,其化学式为 。
(4)Z、W、R形成某种化合物的晶胞结构如右图所示,其化学式为 。
(5)XY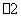 能被酸性KMnO4溶液氧化,其中MnO
能被酸性KMnO4溶液氧化,其中MnO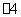 被还原为Mn2+,反应的离子方程式是 。
被还原为Mn2+,反应的离子方程式是 。
 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案科目:高中化学 来源: 题型:
硫代硫酸钠(Na2S2O3)是一种重要的化工产品。某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3·5H2O)。
Ⅰ.【查阅资料】
(1)硫代硫酸钠(Na2S2O3)易溶于水,在中性或碱性环境中稳定,受热、遇酸易分解。
(2)Na2S2O3·5H2O是无色透明晶体,易溶于水,其稀溶液与BaCl2溶液混合无沉淀生成。
(3)向Na2CO3和Na2S混合溶液中通入SO2可制得Na2S2O3(反应方程式为:2Na2S+Na2CO3+ 4SO2===3Na2S2O3+CO2),所得产品常含有少量Na2SO3和Na2SO4。
Ⅱ.【制备产品】实验装置如图所示:


请回答下列问题:
(1)实验步骤:检查装置气密性后,向三颈瓶c中加入Na2CO3和Na2S的混合溶液,再将分液漏斗a中液体滴加到烧瓶b中加热发生反应产生SO2,请写出b中发生反应的化学方程式______________________。待Na2S和Na2CO3完全消耗后,结束反应。过滤c中的混合物,滤液经____________________(填写操作名称)、过滤、洗涤、干燥、得到产品。
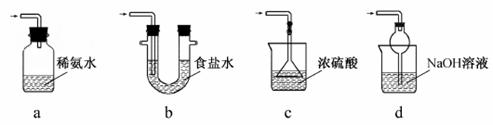
(2) 装置A用于处理尾气,可选用的最合理装置(夹持仪器已略去)为________(填序号)。
(3)为了保证硫代硫酸钠的产量,实验中通入的SO2不能过量,原因是____________________。
III.【测定产品纯度】
准确称取W g产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.100 0 mol·L-1碘的标准溶液滴定。
反应原理为2S2O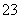 +I2===S4O
+I2===S4O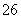 +2I-(忽略Na2SO3与I2反应)
+2I-(忽略Na2SO3与I2反应)
(4)滴定至终点时,溶液颜色的变化:_________________________________。
(5)滴定起始和终点的液面位置如图,则产品的纯度为(设Na2S2O3·5H2O相对分子质量为M)______________。
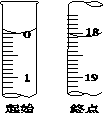
IV.【探究与反思】
(6)为验证产品中含有Na2SO3和Na2SO4,该小组设计了以下实验方案,请将方案补充完整。(所需试剂从稀HNO3、稀H2SO4、稀盐酸、蒸馏水中选择)
取适量产品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,_______________________________,若沉淀未完全溶解,并有刺激性气味的气体产生,则可确定产品中含有Na2SO3和Na2SO4。.
查看答案和解析>>
科目:高中化学 来源: 题型:
用丙醛(CH3-CH2-CHO)制取聚丙烯的过程中发生的反应类型为( )
①取代 ②消去 ③加聚 ④缩聚 ⑤氧化 ⑥还原
A.⑥②③ B.⑤②③ C.①④⑥ D.②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
制备氰氨基化钙的化学方程式为CaCO3+2HCN===CaCN2+CO↑+H2↑+CO2↑,在反应中( )
A.氢元素被氧化,碳元素被还原 B.HCN是氧化剂,不是还原剂
C.CaCN2是氧化产物,H2是还原产物 D.CO是氧化产物,H2是还原产物
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是
A.向Fe(NO3)3溶液中滴入少量的HI溶液:2Fe3++2I-==2Fe2++I2
B.向苯酚钠溶液中通入少量CO2气体:2C6H5O-+CO2+H2O —→2C6H5OH↓+CO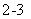
C.Cu(OH)2沉淀溶于氨水得到深蓝色溶液:Cu(OH)2+4NH3== [Cu(NH3)4]2++2OH-
D.澄清石灰水中加入少量NaHCO3溶液:Ca2++2OH-+2HCO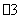 ==CaCO3↓+CO
==CaCO3↓+CO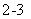 +2H2O
+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
某合作学习小组讨论辨析:
①漂白粉和酸雨都是混合物;
②煤和石油都是可再生能;
③蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质;
④不锈钢和目前流通的硬币都是合金:
⑤硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物;
⑥豆浆和雾都是胶体。
上述说法正确的是
A.①②④⑤ B.①②⑤⑥ C.①③④⑥ D.②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
从硫化物中提取单质锑,经历以下两个过程: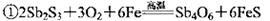
②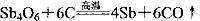 关于反应①、②的说法不正确的是
关于反应①、②的说法不正确的是
A.反应①中Sb元素被氧化
B.反应②中Sb元素被还原
C.标准状况下,每生成4 mol Sb时,消耗67.2LO2
D.反应②说明高温下C的还原性比Sb强
查看答案和解析>>
科目:高中化学 来源: 题型:
脱水环化是合成生物碱类天然产物的重要步骤,某生物碱V合成路线如下:

(1) Ⅱ中含氧官能团的名称 .
(2) 反应②的化学方程式 。
(3)Ⅰ和Ⅲ在浓硫酸催化加热时反应的化学方程式 。
(4) 下列说法正确的是
A. Ⅰ和Ⅴ均属于芳香烃 B. Ⅱ能发生银镜反应
C. Ⅱ能与4molH2发生加成反应 D. 反应③属于酯化反应
(5) A的结构简式 。
(6) Ⅵ与Ⅰ互为同分异构体,Ⅵ遇FeCl3发生显色反应,其苯环上的一氯代物只有2种。写出满足上述条件的Ⅵ的结构简式 。
(7) 一定条件下,化合物Ⅶ(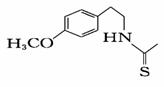 )也能发生类似反应④的环化反应,Ⅶ的环化产物的结构简式 。
)也能发生类似反应④的环化反应,Ⅶ的环化产物的结构简式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
镁是海水中含量较多的金属,镁合金及其镁的化合物用途非常广泛。
(1)Mg2Ni是一种储氢合金,已知:
Mg(s) + H2(g) = MgH2(s) △H1=-74.5kJ·mol-1
Mg2Ni(s) + 2H2(g) = Mg2NiH4(s) △H2=-64.4kJ·mol-1
Mg2Ni(s)+2MgH2(s) = 2Mg(s)+Mg2NiH4(s) 的△H3= ▲ 。
(2)一种用水氯镁石(主要成分为MgCl2·6H2O)制备金属镁工艺的关键流程如下:

①为探究MgCl2•6H2O“一段脱水”的合理温度范围,某科研小组将MgCl2•6H2O在不同温度下分解,测得残留固体物质的X-射线衍射谱图如下图所示(X-射线衍射可用于判断某晶态物质是否存在)。

测得E中Mg元素质量分数为60.0%,则E的化学式为 ▲ 。
“一段脱水”的目的是制备MgCl2·2H2O,温度不高于180 ℃的原因是 ▲ 。
 ②若电解时电解槽中有水分,则生成的MgOHCl与阴极产生的Mg反应,使阴极表面产生MgO钝化膜,降低电解效率。生成MgO的化学方程式为 ▲ 。
②若电解时电解槽中有水分,则生成的MgOHCl与阴极产生的Mg反应,使阴极表面产生MgO钝化膜,降低电解效率。生成MgO的化学方程式为 ▲ 。
③该工艺中,可以循环使用的物质有 ▲ 。
(3)储氢材料Mg(AlH4)2在110-200°C的反应为:
Mg(AlH4)2=MgH2 +2A1+3H2↑
每生成27gAl转移电子的物质的量为 ▲ 。
(4)“镁-次氯酸盐”燃料电池的装置如右图所示,该电池的正极反应式为 ▲ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com