
【题目】在浓CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙(粒子直径在1~10 nm之间)。下图所示A~E为实验室常见的仪器装置(部分固定夹持装置略去),请根据要求回答问题。

(1)实验室选用上图所示装置制取、收集干燥的NH3,接口的连接顺序是:a接_____(填小写字母代号,下同),_____接___,_____接h。
(2)向浓CaCl2溶液中通入NH3和CO2气体制纳米级碳酸钙时,应先通入的气体是____,试写出制纳米级碳酸钙的离子方程式:_____。
(3)在浓CaCl2溶液和NH3用量正确的情况下,CO2不足或过量都会导致纳米级碳酸钙产量下降,若CO2过量,溶液中大量存在的离子有(不考虑弱电解质的电离和盐类水解产生的少量离子):____。
(4)取反应后去除CaCO3的溶液分别做以下实验,下列实验判断合理的是_____(填字母代号)。
A.滴加少量Na2CO3溶液,若有沉淀生成,说明CO2一定不足
B.滴加少量盐酸,若有气泡产生,说明CO2一定过量
C.测量溶液pH,若pH小于7,说明CO2一定过量
D.滴加少量BaCl2溶液,若无沉淀生成,说明CO2一定没有过量
【答案】d e g f NH3 Ca2++2NH3+H2O+CO2===CaCO3+2NH4+ Ca2+、HCO3—、NH4+、Cl- B
【解析】
(1)实验式通常用氯化铵与氢氧化钙加热的条件下制取氨气,并收集干燥的氨气,则连接装碱石灰的装置;氨气的密度小于空气,则应g进f出;最后用E吸收过量的氨气;
(2)为了提高二氧化碳的吸收效果,先通氨气使溶液呈碱性,再通二氧化碳气体;
(3)二氧化碳能与碳酸钙、水反应生成碳酸氢钙;
(4) A.若二氧化碳过量时,溶液存在Ca2+,滴加少量Na2CO3溶液,有沉淀生成;
B.滴加少量盐酸,若有气泡产生,则溶液中存在HCO3-;
C.无论二氧化碳过量与否,溶液主要为氯化铵,溶液显酸性;
D.无论二氧化碳过量与否,滴加少量BaCl2溶液,均无沉淀生成。
(1)实验式通常用氯化铵与氢氧化钙加热的条件下制取氨气,题目要求收集干燥的氨气,则连接装置C,其为碱石灰,起干燥作用应d进e出;氨气的密度小于空气,则应g进f出;最后用E吸收过量的氨气,其易溶于水,则用防倒吸装置;
(2)为了提高二氧化碳的吸收效果,应先通氨气,使溶液呈碱性,再通二氧化碳气体,制取纳米级碳酸钙的离子方程式为Ca2++2NH3+H2O+CO2===CaCO3+2NH4+;
(3)二氧化碳能与碳酸钙、水反应生成碳酸氢钙,CO2过量时,导致碳酸钙变为碳酸氢钙,则溶液中存在大量的钙离子、碳酸氢根离子,和未参与反应的铵根离子、氯离子;
(4) A.若二氧化碳过量时,溶液存在Ca2+,滴加少量Na2CO3溶液,有沉淀生成,不能判断CO2是否足量,A错误;
B.滴加少量盐酸,若有气泡产生,则溶液中存在HCO3-,说明CO2一定过量,B正确;
C.无论二氧化碳过量与否,溶液主要为氯化铵,溶液显酸性,测量溶液pH小于7,不能说明CO2一定过量,C错误;
D.无论二氧化碳过量与否,滴加少量BaCl2溶液,均无沉淀生成,不能说明CO2一定没有过量,D错误;
答案为B。


科目:高中化学 来源: 题型:
【题目】某同学进行下列实验:
装置 | 操作 | 现象 |
| 将盛有浓硝酸的烧杯A放入盛有淀粉KI溶液的烧杯C中,然后将铜片放入烧杯A后,立即用烧杯B罩住。 | 烧杯A液体上方立即出现大量红棕色气体;一段时间后,红棕色气体消失,烧杯A和C中的液体都变成蓝色。 |
下列说法不合理的是
A.烧杯A中发生反应:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
B.红棕色气体消失可能与NO2和烧杯C中的KI发生反应有关
C.烧杯A中溶液变蓝是因为产生了Cu(NO3)2
D.若将铜片换成铁片,则C中的液体不会变蓝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )。
A.在离子化合物中,只存在离子键,没有共价键
B.非极性键只存在于双原子的单质分子(如![]() )中
)中
C.原子序数为11与9的元素能够形成离子化合物
D.由不同元素组成的含多个原子的分子中,只存在极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是(NA表示阿伏加德罗常数的值) ( )
A. 在常温常压下,11.2 L N2含有的原子数为NA
B. 32 g O2在标准状况下所占体积约为22.4 L
C. 标准状况下,18 g H2O所占的体积约为22.4 L
D. 在同温同压下,相同体积的任何气体单质所含的原子数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图A、B、C、D、E、F等几种常见有机物之间的转化关系图,其中A是面粉的主要成分;C和E反应能生成F,F具有香味。
![]()
在有机物中,凡是具有—CHO结构的物质,具有如下性质:
(1)与新制氢氧化铜悬浊液反应,产生砖红色沉淀;
(2)在催化剂作用下, —CHO被氧气氧化为—COOH,即![]() 。
。
根据以上信息及各物质的转化关系完成下列各题。
(1)B的化学式为_________,C的结构简式为__________。
(2)其中能与新制氢氧化铜悬浊液反应产生砖红色沉淀的物质有_________(填名称)。
(3)C→D的化学方程式为______________。
(4)C + E→ F的化学方程式为 ______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若它们的温度和密度均相同,试根据甲、乙的摩尔质量![]() 关系,判断下列说法正确的是( )
关系,判断下列说法正确的是( )
A.若![]() ,则气体的压强:甲
,则气体的压强:甲![]() 乙
乙
B.若![]() ,则气体的摩尔体积:甲
,则气体的摩尔体积:甲![]() 乙
乙
C.若![]() ,则气体体积:甲
,则气体体积:甲![]() 乙
乙
D.若![]() ,则分子数:甲
,则分子数:甲![]() 乙
乙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定稳定下,在容积不变的密闭容器中,进行如下可逆反应:![]() ,下列能表明该反应已达到平衡状态的是
,下列能表明该反应已达到平衡状态的是
①![]()
②![]()
③![]()
④混合气的密度保持不变
⑤混合气体的平均摩尔质量不变
A.仅④B.仅④⑤
C.仅①④D.仅③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是实验室进行氨溶于水的“喷泉实验”的装置,下列叙述不正确的是( )
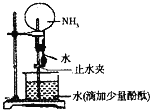
A.该实验说明氨气是一种极易溶于水的气体
B.进入烧瓶中的液体颜色由无色变为红色,说明氨水有碱性
C.氨水很稳定,将烧瓶中的红色溶液加热,颜色不会发生变化
D.形成“喷泉”的主要原因是氨气溶于水后,烧瓶内的气压小于大气压
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化氢和臭氧是用途很广的氧化剂。试回答下列问题:
(1)过氧化氢是一种绿色氧化剂,写出在酸性条件下H2O2氧化氯化亚铁的离子反应方程式:____________________________________
(2)Na2O2、K2O2、 以及BaO2都可与酸作用生成过氧化氢,目前实验室制取过氧化氢可通过上述某种过氧化物与适量稀硫酸作用,过滤即可制得。最适合的过氧化物是____________(写电子式),
臭氧(O3)可以使湿润的淀粉-碘化钾试纸变蓝,反应的化学方程式为:
KI+O3+H2O→KOH+I2+O2(未配平 ) 回答问题:
① 还原产物的化学式为_____________
② 配平后的化学方程式是________________________________
(4)O3 可由臭氧发生器(原理如下图所示)电解稀硫酸制得。

①图中阴极为_____(填“A”或“B”)。
② 若C处不通入O 2 ,D、E处分别收集到11.2L和有4.48L
气体(标准状况下), 则E处收集的气体中O3所占的体积分数
为__________(忽略 O 3 的分解)。
③ 若C处通入O 2,则A极的电极反应式为:____________。
(5)新型O3氧化技术对燃煤烟气中的NOx和SO2脱除效果显著,锅炉烟气中的NOx 95%以上是以NO形式存在的,可发生反应NO(g)+ O3(g)![]() NO2(g)+ O2 (g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应 ,正反应速率随时间变化的示意图(如下图)所示。由图可得出的正确说法是___________
NO2(g)+ O2 (g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应 ,正反应速率随时间变化的示意图(如下图)所示。由图可得出的正确说法是___________

a.反应在c点达到平衡状态
b.反应物浓度:b点小于c点
c.反应物的总能量低于生成物的总能量
d.Δt1=Δt2时,NO的转化率:a~b段小于b~c段
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com