
| A. | 同温同压下,H2 (g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H不相同 | |
| B. | 用pH试纸测定新制氯水的pH | |
| C. | 已知:①2H2(g)+O2(g)═2H2O (g)△H1 ②2H2(g)+O2 (g)═2H2O(1)△H2,则△H1<△H2 | |
| D. | 在中和滴定实验中,用待测NaOH溶液润洗锥形瓶,测定结果将偏高 |
分析 A、反应热与条件无关;
B、新制氯水有漂白性;
C、对于放热反应,当反应物能量相同时,生成物的能量越低,放出的热量越多;
D、在中和滴定实验中,用待测NaOH溶液润洗锥形瓶,待测液的物质的量将增多.
解答 解:A、反应热取决于反应物和生成物总能量的相对大小,与条件无关,故此反应无论在光照还是在点燃条件下,△H均相同,故A错误.;
B、新制氯水有漂白性,故对pH有漂白性,不能准确测出溶液的pH,故B错误;
C、对于放热反应,当反应物能量相同时,生成物的能量越低,放出的热量越多,由于液态水的能量更低,故第二个反应放出的热量更多,△H2<△H1,故C错误;
D、在中和滴定实验中,用待测NaOH溶液润洗锥形瓶,待测液的物质的量将增多,会导致消耗的酸的物质的量偏多,带入公式计算出的氢氧化钠的浓度将偏高,故D正确;
故选D.
点评 本题考查了反应热与反应物、生成物总能量之间的关系,反应热取决于反应物与生成物总能量的相对大小,当反应物的总能量大于生成物的总能量,该反应就放热,否则吸热,与反应条件无关,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 保存氢氧化钠溶液,常用带橡胶塞的玻璃瓶 | |
| B. | 保存浓硝酸,常用带玻璃塞的棕色试剂瓶 | |
| C. | 保存金属铝时,常在试剂瓶中加入煤油进行封存 | |
| D. | 保存氢氟酸时,常用塑料瓶而不用玻璃瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 离子 | Mg2+ | Al3+ | Cl- | X |
| 物质的量浓度 | a | 2a | 2a | b |
| A. | Na+、6a | B. | SO42-、3a | C. | OH-、6a | D. | CO32-、4a |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
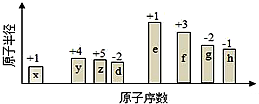 随原子序数的递增,八种短周期元素(用字母表示)原子半径的相对大小、最高正价或最低负价的变化如图所示.根据判断出的元素回答下列问题:
随原子序数的递增,八种短周期元素(用字母表示)原子半径的相对大小、最高正价或最低负价的变化如图所示.根据判断出的元素回答下列问题: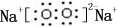 ;B是常见的液态化合物,其稀溶液易被催化分解,可使用的催化剂为AB.(填序号)
;B是常见的液态化合物,其稀溶液易被催化分解,可使用的催化剂为AB.(填序号)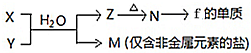
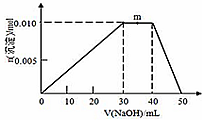
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
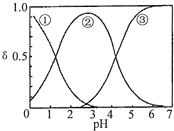 H2C2O4水溶液中H2C2O4、HC2O4-和C2O42-三种形态的粒子的分布分数δ随溶液pH变化的关系如图所示,下列说法正确的是( )
H2C2O4水溶液中H2C2O4、HC2O4-和C2O42-三种形态的粒子的分布分数δ随溶液pH变化的关系如图所示,下列说法正确的是( )| A. | 曲线①代表的粒子是HC2O4- | |
| B. | 0.1 mol•L-1 NaHC2O4溶液中:c(Na+)=c(C2O42-)+c(H2C2O4)+c(HC2O4-) | |
| C. | pH=5时,溶液中主要含碳微粒浓度大小关系为:c(C2O42-)>c(H2C2O4)>c(HC2O4-) | |
| D. | 在一定温度下,往CaC2O4饱和溶液中加入少量CaCl2固体,c(Ca2+)不变,c(C2O42-)将减小.(CaC2O4难溶于水) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,100g 17%H2O2水溶液中含氧原子总数为NA | |
| B. | 常温常压下,2.8g N2气体分子中所含的共用电子对数目为0.3NA | |
| C. | 0.2mol/L的NaCl溶液中含有的Cl-数是0.2NA | |
| D. | 在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com