
【题目】如图为铜片与浓硝酸反应的装置示意图,据图回答下列问题: 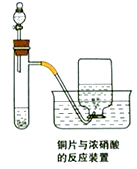
(1)写出试管内发生反应的化学方程式;
(2)描述在实验过程中观察到的颜色变化: 试管内液体呈色;试管内液体上方气体呈色;集气瓶内收集到的气体呈色.
(3)在反应一段时间后,从分液漏斗处向试管内加入蒸馏水,请描述加水后试管内和集气瓶内颜色的变化情况:试管内液体呈色;试管内液体上方气体呈色.
【答案】
(1)Cu+4HNO3 (浓)=Cu(NO3)2+2NO2↑+2H2O
(2)绿;红棕;无
(3)蓝;无
【解析】解:(1)硝酸具强氧化性,能把不活泼的金属铜氧化成铜离子,同时被还原成二氧化氮,化学方程式为:Cu+4HNO3 (浓)=Cu(NO3)2+2NO2↑+2H2O;所以答案是:Cu+4HNO3 (浓)=Cu(NO3)2+2NO2↑+2H2O;(2)试管内的溶液是硝酸铜溶液,铜与浓硝酸反应后溶液颜色呈现绿色.原因是产生的红棕色二氧化氮气体一部分溶解在溶液中呈黄色,而溶液中[Cu(H2O)4]2+呈蓝色,两者的混合色为绿色;试管内液体上方的气体是二氧化氮,二氧化氮呈红棕色,所以试管内液体上方的气体呈红棕色;二氧化氮气体和水反应生成无色气体NO,3NO2+H2O=2HNO3+NO,所以集气瓶内收集到的气体呈无色.所以答案是:绿;红棕;无;(3)从分液漏斗处向试管内加入蒸馏水,二氧化氮气体和水反应,溶液呈现铜离子的颜色,所以试管内液体是蓝色;3NO2+H2O=2HNO3+NO,NO是无色的,所以试管内液体上方气体呈无(或红棕色变浅)色.所以答案是:蓝;无(或红棕色变浅).


 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:
【题目】海带中含有丰富的碘.为了从海带中提取碘,某研究性学习小组设计并进行了以下实验: 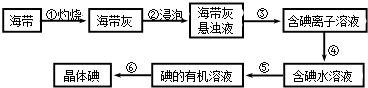
(1)步骤③的实验操作名称是;步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是 .
(2)步骤④需加入的试剂是 , 反应的离子方程式是 .
(3)步骤⑤中,某学生选择用苯来提取碘,理由是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过一步反应不能直接完成的是( )
①N2→NO2②S→SO2 ③NH3→NO④NO→HNO3⑤CuSO4→Cu(NO3)2⑥SiO2→H2SiO3 .
A.①⑥
B.④⑤
C.①④
D.⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】mA(s)+nB(g)qC(g);△H<0的可逆反应,在一定温度下的密闭容器中进行,平衡时B的体积分数V(B)%与压强(P)关系如图所示,下列叙述正确的是( ) 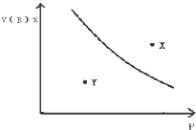
A.m+n<q
B.n<q
C.X点时的状态,V正>V逆
D.X点比Y点混和物的正反应速率慢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究或认识物质的化学性质一般可从以下几个方面入手(以SiO2为例)。
(1)从物质分类角度分析可能具有的通性,如酸性、碱性等。
SiO2属于__________氧化物(填“酸性”“碱性”或“两性”)。盛装NaOH 等碱性溶液的试剂瓶不能用玻璃塞,其原因可用离子方程式表示为____________________________。
(2)从核心元素化合价角度分析可能具有氧化性、还原性。
①据SiO2中Si元素的价态可推知SiO2_____________(填字母):
A.只有还原性 B.只有氧化性 C.既有还原性又有氧化性
②工业上用石英砂和焦炭混合高温制取粗硅,其反应为:SiO2+2C![]() Si+2CO↑
Si+2CO↑
用双线桥法标出电子转移方向与数目:____________________________。
(3)从其它角度认识可能具有的特性。
SiO2能与唯一的酸____________ (填物质名称或化学式)反应,工艺上常利用该反应___________(填一种用途)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】体积为V mL,密度为d g/mL,溶质的摩尔质量为M g·mol-1,物质的量浓度为c mol·L-1,溶质的质量分数为a%,溶质的质量为m g。下列式子正确的是
A. m=a V/(100d) B. c=1000da/M
C. c=1000m/(VM) D. a%=[cM/(1000d)]%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将下列物质按酸、碱、盐分类排列,正确的是( )
A. 硝酸、苏打、石灰石 B. 硅酸、纯碱、食盐
C. 盐酸、乙醇、氯化钠 D. 硫酸、烧碱、小苏打
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中发生反应H2(g)+I2(g)2HI(g),0~5min内H2的浓度减少了0.1mol/L,则在这段时间内
用HI表示的平均反应速率为( )
A.0.01molL﹣1min﹣1
B.0.04molL﹣1min﹣1
C.0.2molL﹣1min﹣1
D.0.5molL﹣1min﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略)。
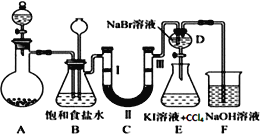
(1)装置 A 中反应的化学反应方程式为:________________________________。装置 B 中饱和食盐水的作用是___________________;同时装置 B 亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时 B 中的现象________________________________。
(2)装置 C 的实验目的是验证氯气是否具有漂白性,为此 C 中Ⅰ、Ⅱ、Ⅲ依次放入_____________。(填序号)
a | b | c | d | |
Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(3)设计装置 D、 E 的目的是验证氯、溴、碘单质的氧化性强弱(Cl2> Br2>I2),当向D中缓缓通入少量氯气时,可以看到无色溶液逐渐变为橙黄色,说明Cl2氧化性>Br2,打开活塞,将装置D中少量溶液加入装置 E中,振荡,观察到的现象是________________________________。
(4)工业上将氯气通入石灰乳制取漂白粉, 化学反应方程式为_____________________________,漂白粉敞放于空气中会失效,请写出失效所发生反应的化学方程式_____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com