
【题目】【2014 Ⅱ卷】下列反应中,反应后固体物质增重的是
A.氢气通过灼热的CuO粉末 B.二氧化碳通过Na2O2粉末
C.铝与Fe2O3发生铝热反应 D.将锌粒投入Cu(NO3)2溶液
【答案】B
【解析】本题的解题要点是首先理清反应过程的相关反应,根据反应方程式判断相关物质的质量变化;其次要认真审题,审清“固体”、“增重”等关键词语,逐项分析。A、氢气通过灼热的CuO粉末发生的反应为CuO+H2![]() Cu+H2O,固体由CuO变为Cu,1molCuO的质量为80g,1molCu的质量为64g,反应后固体质量减小,错误;B、二氧化碳通过Na2O2粉末发生的反应为2Na2O2+2CO2====2Na2CO3+O2,固体由Na2O2变为Na2CO3,1mol Na2O2的质量为78g,1mol Na2CO3的质量为106g,反应后固体质量增加,正确;C、铝与Fe2O3发生铝热反应,化学方程式为2Al+Fe2O3
Cu+H2O,固体由CuO变为Cu,1molCuO的质量为80g,1molCu的质量为64g,反应后固体质量减小,错误;B、二氧化碳通过Na2O2粉末发生的反应为2Na2O2+2CO2====2Na2CO3+O2,固体由Na2O2变为Na2CO3,1mol Na2O2的质量为78g,1mol Na2CO3的质量为106g,反应后固体质量增加,正确;C、铝与Fe2O3发生铝热反应,化学方程式为2Al+Fe2O3![]() Al2O3+2Fe,反应前后各物质均为固体,根据质量守恒定律知,反应后固体质量不变,错误;D、将锌粒投入Cu(NO3)2溶液发生的反应为Zn + Cu(NO3)2 ==== Zn(NO3)2+ Cu,固体由Zn变为Cu,1mol Zn的质量为65g,1molCu的质量为64g,反应后固体质量减小,错误。
Al2O3+2Fe,反应前后各物质均为固体,根据质量守恒定律知,反应后固体质量不变,错误;D、将锌粒投入Cu(NO3)2溶液发生的反应为Zn + Cu(NO3)2 ==== Zn(NO3)2+ Cu,固体由Zn变为Cu,1mol Zn的质量为65g,1molCu的质量为64g,反应后固体质量减小,错误。


科目:高中化学 来源: 题型:
【题目】将Cu投入足量的FeCl3的水溶液中,两者发生反应的化学方程式如下:2FeCl3+Cu2FeCl2+CuCl2
(1)请用双线桥法标出电子转移的方向和数目_______。
(2)当有0.3 mol电子发生转移时,发生反应的Cu的质量为_________。
(3)请将以上反应改写为离子方程式___________________。
(4)配平下列方程式: FeCl2+ H2O2+ HCl— FeCl3+ H2O
______________________
(5)高锰酸钾和氢溴酸溶液可以发生下列反应:2KMnO4+16HBr5Br2+2MnBr2+2KBr+8H2O,若消耗15.8 g氧化剂KMnO4,则被氧化的还原剂的质量是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苹果汁是人们喜爱的饮料,由于此饮料中含有Fe2+ , 现榨的苹果汁在空气中会由Fe2+变为Fe3+ . 若榨汁时加入维生素C,可有效防止这种现象的发生.这说明维生素C具有( )
A.还原性
B.氧化性
C.碱性
D.酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是( )
A. 工业生产硫酸的过程中使用过量的氧气,以提高二氧化硫的转化率;
B. 合成氨工厂通常采用20MPa~50MPa压强,以提高原料的利用率;
C. 在实验室里,可用碳酸钙粉末和稀硫酸制得二氧化碳气体;
D. 实验室用排饱和食盐水的方法收集氯气。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质能通过化合反应直接制得的是( ) ①FeCl2 ②FeCl3 ③Fe(OH)3 ④HCl.
A.只有①②③
B.只有②③
C.只有①③④
D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E、F六种短周期的元素,原子序数依次增大,其中A、D元素的原子最外电子层均只有一个电子,且A是所有元素中原子半径最小的;C、F同主族,B元素位于元素周期表中第二周期,且原子最外层电子数占核外电子总数的3/4,F元素原子最外电子层比同周期的E元素原子的最外电子层多4个电子,E的最高价氧化物对应的水化物既能溶于强酸又能溶于强碱。请问答以下问题:
(1)写出C的元素符号_____,写出F在元素周期表中的位置_______。
(2)写出B、D、E三种元素组成的常见化合物的名称___________。
(3)写出E、F两种元素最高价氧化物对应水化物相互反应的离子方程式_______________。(4)工业生产E的化学方程式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【加试题】乳酸亚铁:{[CH3CH(OH)COO]2Fe·3H2O,M=288.0g/mol}是一中新型的优良补铁剂,绿白色晶体,溶于水,几乎不溶于乙醇。某研究性学习小组欲从硫铁矿烧渣(主要成分为Fe2O3、SiO2、Al2O3)出发,先制备绿矾,再合成乳酸亚铁。
已知:
①几种金属离子生成氢氧化物沉淀的PH(开始沉淀的PH按金属离子浓度为1.0mol/L计算)。
金属离子 | 开始沉淀的PH | 沉淀完全的PH |
Fe3+ | 1.1 | 3.2 |
Al3+ | 3.0 | 5.0 |
Fe2+ | 5.8 | 8.8 |
②研究性学习小组设计的由烧渣制备绿矾晶体的操作流程如下:
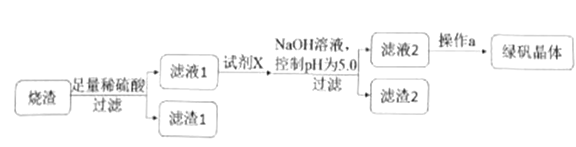
③由绿矾(FeSO4·7H2O)制备乳酸亚铁涉及下列反应:
FeSO4+Na2CO3=FeCO3↓+Na2SO4
2CH3CH(OH)COOH+FeCO3+2H2O![]() [CH3CH(OH)COO]2Fe·3H2O+CO2↑。
[CH3CH(OH)COO]2Fe·3H2O+CO2↑。
请回答:
(1)滤渣2的成分为__________(写化学式)。
(2)操作a为蒸发浓缩、冷却结晶、抽滤、洗涤、干燥。洗涤绿矾粗产品的具体操作为_______。
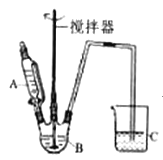
(3)据题干信息,欲制备较纯净的FeCO3时,某同学设计的实验装置示意图如图所示(夹持装置省略)。仪器A 中存放的试剂为________,装置C的作用为___________。
(4)在室温下,将所得的乳酸亚铁成品用无水乙醇进行浸泡2次,从而得到精制产品。选择用无水乙醇进行浸泡的优点是___________(写出两点)。
(5)该学习小组同学用KMnO4滴定法测定样品中Fe2+的量进而计算产品中乳酸亚铁的纯度,发现结果总是大于100%,其原因可能是___________。
经查阅文献后,小组同学改用Ce(SO4)2标准溶液滴定进行测定。反应中Ce4+离子的还原产物为Ce3+。测定时,先称取0.576g样品,溶解后进行必要处理,用0.1000mol/L Ce(SO4)2标准溶液滴定至终点,记录数据如下表。
滴定次数 | 0.1000mol/L Ce(SO4)2标准溶液体积/mL | |
滴定前读数 | 滴定后读数 | |
1 | 0.10 | 19.85 |
2 | 0.12 | 21.32 |
3 | 1.05 | 20.70 |
则产品中乳酸亚铁的纯度为________(以质量分数表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将V1 mL 1.00 mol·L-1 HCl溶液和V2 mL 未知浓度的NaOH溶液混合均匀后,测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL)。
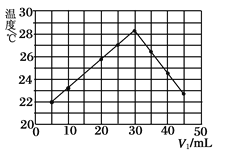
下列叙述正确的是
A.做该实验时环境温度为22 ℃
B.该实验表明化学能可以转化为热能
C.NaOH溶液的浓度约为1.00 mol·L-1
D.该实验表明有水生成的反应都是放热反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com