
【题目】下列物质能通过化合反应直接制得的是( ) ①FeCl2 ②FeCl3 ③Fe(OH)3 ④HCl.
A.只有①②③
B.只有②③
C.只有①③④
D.全部
 优等生题库系列答案
优等生题库系列答案科目:高中化学 来源: 题型:
【题目】下列反应中属于氧化还原反应,但水既不作氧化剂又不作还原剂的是
A.SO3+H2O===H2SO4
B.2Na2O2+2H2O===4NaOH+O2↑
C.2F2+2H2O===4HF+O2
D.2Na+2H2O===2NaOH+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应3A(g)![]() 3B(?)+C(?) △H>0达到化学平衡后,
3B(?)+C(?) △H>0达到化学平衡后,
(1)升高温度,用“变大”、“变小”、“不变”或“无法确定”填空。
①若B、C都是气体,气体的平均相对分子质量 ;
②若B、C都不是气体,气体的平均相对分子质量 ;
③若B是气体,C不是气体,气体的平均相对分子质量 ;
(2)如果平衡后保持温度不变,将容器体积增加一倍,新平衡时A的浓度是原来的60%,则B是 态,C是 态。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组利用下图装置探究温度对CO还原Fe2O3的影响(固定装置略)
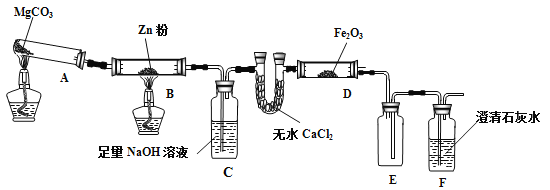
(1)MgCO3的分解产物为 。
(2)装置C的作用是 ,处理尾气的方法为 。
(3)将研究小组分为两组,按图装置进行对比实验,甲组用酒精灯、乙组用酒精喷灯对装置D加热,反应产物均为黑色粉末(纯净物),两组分别用产物进行以下实验。(Fe2+ 遇K3[Fe(CN)6]溶液会生成蓝色沉淀)
步骤 | 操作 | 甲组现象 | 乙组现象 |
1 | 取黑色粉末加入稀盐酸 | 溶解,无气泡 | 溶解,有气泡 |
2 | 取步骤1中溶液,滴加K3[Fe(CN)6]溶液 | 蓝色沉淀 | 蓝色沉淀 |
3 | 取步骤1中溶液,滴加KSCN溶液 | 变红 | 无现象 |
4 | 向步骤3溶液中滴加新制氯水 | 红色褪去 | 先变红,后褪色 |
①乙组得到的黑色粉末是 。
②甲组步骤1中反应的离子方程式为 。
③乙组步骤4中,溶液变红的原因为 ;溶液褪色可能的原因为 。
④从实验安全考虑,题图装置还可采取的改进措施是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列反应的化学方程式,判断有关物质的还原性强弱
①2Fe2++Cl2═2Fe3++2Cl﹣
②I2+SO2+2H2O═H2SO4+2HI
③2Fe3++2I﹣═2Fe2++I2
A. SO2>I﹣>Fe2+>Cl﹣
B. I﹣>Fe2+>Cl﹣>SO2
C. Cl﹣>Fe2+>SO2>I﹣
D. Fe2+>I﹣>Cl﹣>SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2014 Ⅱ卷】下列反应中,反应后固体物质增重的是
A.氢气通过灼热的CuO粉末 B.二氧化碳通过Na2O2粉末
C.铝与Fe2O3发生铝热反应 D.将锌粒投入Cu(NO3)2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 容量瓶和分液漏斗使用前必须要检漏并干燥
B. 蒸馏操作时,温度计水银球应插入液面下
C. 检验Fe2+、Fe3+、Cl-溶液中的Fe2+,加入酸性高锰酸钾看是否褪色
D. 做过碘升华的圆底烧瓶可以用酒精洗涤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z四种元素在周期表中的位置如图所示,下列说法不正确的是
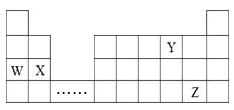
A. W、X、Y三种元素的原子半径依次减少
B. W元素的最高价氧化物的水化物的碱性比X的强
C. 可在省略号对应的族区域寻找各种优良的催化剂
D. Z元素与水反应得到HZO,HZO只有氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有48.4g碱式碳酸镁样品(化学式:xMgCO3·yMg(OH)2·zH2O,x、y、z为正整数),将其分为二等份,一份样品充分灼烧至恒重进行热重分析,结果如图所示。另一份投入150mL某溶液的盐酸中,充分反应后生成CO24.48L(已知算成标准状况下),所得溶液稀释至250mL,测得溶液的c(H+)=0.100mol/L。

按要求回答下列问题:
(1)盐酸的物质的量浓度c(HCl)=______mol/L
(2)x:y:z=______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com